<strong>PRODUÇÃO, COMPOSIÇÃO QUÍMICA E QUALIDADE DA BEBIDA DE CAFÉ ARÁBICA EM RAZÃO DA DOSE DE COBRE E ZINCO </strong>

O cobre e o zinco embora exigidos em pequenas quantidades pelo cafeeiro são essenciais na constituição e na ativação de varias enzimas, atuando na oxidação de compostos fenólicos, formação de lignina, síntese de aminoácidos, carboidratos e de proteínas. Tais compostos estão diretamente relacionados à qualidade química dos grãos crus do café e por isso podem influenciar na qualidade da bebida. Objetivou-se com o presente trabalho avaliar a influência do cobre e do zinco na composição química dos grãos e na qualidade de bebida do café. O experimento foi conduzido em casa de vegetação do Departamento de Fitotecnia (UFV-MG), em sistema hidropônico com os tratamentos arranjados em delineamento inteiramente casualizado, com três repetições, sendo cada parcela constituída por 2 vasos, contendo uma planta de cafeeiro em cada vaso. Os tratamentos consistiram de doses crescentes de cobre (0,05; 0,1; 0,2; 0,4 e 0,8 µmol L-1) e de zinco (0,5; 1,0; 2,0; 3,0 e 4,0 µmol L-1) em solução nutritiva. Foram colhidos grãos maduros de cada tratamento, e após sua secagem e beneficiamento determinaram-se: a atividade da PPO, e os teores de cafeína, trigonelina, fenóis totais, ácido 5-cafeoilquinico (5-CQA) e sacarose. Verificaram-se incrementos lineares com o incremento das doses de Cu, e resposta quadrática para as doses de Zn na atividade da enzima PPO e nos teores de sacarose, respectivamente. Os teores de trigonelina apresentaram resposta quadrática às doses de Cu e de Zn, para os teores de cafeína observou-se efeito quadrático apenas para as doses de Zn. Fenóis totais e 5-CQA sofreram redução segundo função de base raiz quadrada até um ponto de mínimo, com posterior incremento com as doses dos nutrientes em estudo. As doses de Cu e Zn via solução nutritiva influenciaram positivamente a atividade da PPO, os teores de sacarose e trigonelina, e negativamente fenóis totais e 5-CQA, atributos relacionados à qualidade dos grãos de café. Os teores foliares que se relacionaram aos pontos de máximo ou mínimo dos atributos de qualidade estudados variaram entre 4,51 e 5,8 mg kg-1 de Cu e 8,0 e 12,7 mg kg-1 de Zn.

INTRODUÇÃO GERAL
Dentro do contexto do agronegócio brasileiro, a cafeicultura desempenha importante papel na economia, pois contribui com cerca de 2,9% do valor total das exportações nacionais. Segundo o Conselho dos Exportadores de Café do Brasil (CECAFÉ), em 2013 as exportações de café atingiram 31,22 milhões de sacas de 60 kg, crescimento de 10,2%, em relação a 2012, registrando uma receita de US$ 5,15 bilhões.
A previsão atual para a produção nacional de café beneficiado é de 48,34 milhões de sacas. O resultado representa uma redução de 1,6%, ou de 0,81 milhões de sacas, quando comparado com a safra anterior (CONAB, 2014).
A cultura do cafeeiro é uma atividade, tanto sob o ponto de vista econômico, quanto pelo aspecto social, que gera emprego e renda, sobretudo quando se consideram as demais atividades ao longo de toda a cadeia produtiva (VIANA, 2003). No Brasil é a segunda bebida mais consumida, atrás apenas da água, com um consumo per capita de 6,4 kg/habitante ano, onde encontra consumidores cada dia mais exigentes em qualidade, com um paladar mais apurado, além de atentos para a produção econômica e ambientalmente sustentável (ABIC, 2012).
Essas exigências por cafés de melhor qualidade, tanto no mercado nacional, quanto no mercado internacional estão sendo responsáveis pela difusão e adoção de novas tecnologias de produção e preparação. Um dos fatores que determinaram o declínio brasileiro no mercado internacional foi a falta de qualidade do produto nacional (MARTINS et al., 2005). A qualidade da bebida é avaliada pelo aroma, corpo, acidez e suavidade, cor e aspecto homogêneos. Baseado nessas características, o café é dividido em sete classes decrescentes de qualidade: bebida estritamente mole, mole, apenas mole, duro, riado, rio e rio zona (POLTRONIERI et al., 2011).
A qualidade dos produtos agrícolas não é facilmente definida ou medida, como se faz para a produção. O padrão de qualidade depende do propósito pelo qual a planta ou parte dela é utilizada (MENGEL e KIRKBY, 1987). No caso do cafeeiro, o seu estado nutricional certamente correlaciona-se com a qualidade da bebida, pois interfere na produção e proporção de compostos químicos desejáveis ou indesejáveis nos grãos. Desse modo, compreender o efeito dos nutrientes sobre a qualidade do café é necessário pois segundo Silva et al. (2002) a melhoria da qualidade do grão tem muita influência no preço final de mercado.
No entanto, a composição química dos grãos é influenciada por fatores genéticos, ambientais e culturais, pelos métodos de colheita, processamento, armazenamento, torração e moagem, que afetam diretamente a qualidade da bebida do café (MENDONÇA et al. 2005). Em se tratando das condições de manejo, as adubações e o estado nutricional da planta podem influenciar tanto na produção, quanto na composição do grão cru e, consequentemente, a qualidade da bebida.
Embora o café seja um dos produtos agrícolas mais estudados no Brasil, e um dos principais produtos da pauta de exportação brasileira, seu valor comercial depende da qualidade e entre os fatores que precisam ser pesquisados está a relação entre a nutrição e a qualidade do grão e da bebida do café.
Apesar de importante, há pouca informação científica sobre a influência dos nutrientes na qualidade dos grãos produzidos, limitando-se às referências, a doses de potássio na produção e qualidade do grão de café (SILVA et al. 1999; SILVA et al. 2002), diferentes fontes e doses de N sobre a produção e qualidade do café (MALTA et al. 2003), nutrição nitrogenada e potássica afetando a qualidade da bebida (CLEMENTE, 2010).
Em relação aos micronutrientes e sua influencia na formação de compostos nos grãos e na qualidade da bebida do café, pouca importância tem sido dada, limitando-se suas referências à utilização de doses de zinco na qualidade da bebida do café (POLTRONIERI et al., 2011; MARTINEZ et al., 2013).
Mediante o exposto, percebe-se a necessidade de se pesquisar a relação entre a nutrição mineral com micronutrientes e a qualidade da bebida do café, entre os quais o cobre e o zinco, pois esses nutrientes já foram estudados no crescimento e na produção do cafeeiro.
CAPÍTULO 1
COMPOSIÇÃO QUÍMICA E QUALIDADE DE CAFÉ ARÁBICA SUBMETIDO A DOSES DE ZINCO
O zinco embora exigido em pequenas quantidades pelo cafeeiro é essencial na constituição e na ativação de varias enzimas, atuando na síntese de aminoácidos, carboidratos e de proteínas. Tais compostos estão diretamente relacionados à qualidade química dos grãos crus de café e, por isso, podem influenciar na qualidade da bebida. Objetivou-se com o presente trabalho avaliar a influência do Zn na composição química dos grãos e na qualidade de bebida do café. O experimento foi conduzido em casa de vegetação do Departamento de Fitotecnia (UFV-MG), em sistema hidropônico com os tratamentos arranjados em delineamento inteiramente casualizado, com três repetições, sendo cada parcela constituída por 2 vasos, contendo uma planta de cafeeiro em cada vaso. Os tratamentos consistiram de doses crescentes de Zn (0,5; 1,0; 2,0; 3,0 e 4,0 µmol L-1) em solução nutritiva, mais um tratamento adicional que recebeu solução nutritiva contendo 0,5 µmol L-1 de Zn via solução, e 12 pulverizações foliares com sulfato de Zn a 0,2%. Foram colhidos os grãos maduros de cada tratamento, e após sua secagem e beneficiamento determinaram-se: Acidez total titulável (ATT), fenóis totais, ácido 5-cafeoilquinico (5-CQA), a atividade da polifenoloxidase (PPO), os teores de sacarose, cafeína, trigonelina, K lixiviado, condutividade elétrica e analise sensorial. Verificaram-se respostas quadráticas para as doses de Zn nos dois anos de avaliação na ATT, atividade da enzima PPO, nos teores de sacarose e cafeína. Os teores de trigonelina no primeiro ano apresentaram resposta segundo a função raiz quadrada e no segundo ano resposta quadrática às doses de Zn. Fenóis totais e 5-CQA sofreram redução segundo a função raiz quadrada até um ponto de mínimo, com posterior incremento. As doses de Zn via solução nutritiva e pulverização foliar influenciaram positivamente a atividade da PPO, os teores de sacarose e trigonelina, e negativamente fenóis totais e 5-CQA, atributos relacionados à qualidade dos grãos de café. Os teores foliares que se relacionaram aos pontos de máximo ou mínimo dos atributos de qualidade estudados variaram entre 8,0 e 12,7 mg kg-1 de Zn.
INTRODUÇÃO
A composição química dos grãos do café como também as suas variações qualitativas e quantitativas, são analisadas por diversos pesquisadores, em função das espécies estudadas, dos efeitos isolados do processamento, do ambiente de cultivo e do manejo (AVELINO et al., 2005; CAMPA et al., 2005; DUARTE et al., 2010; KNOPP et al., 2006; MONTEIRO; FARAH, 2012; RIBEIRO, 2013). Dentre os componentes físico-químicos do grão cru do café, os isômeros do ácido clorogênico (3-CQA, 4-CQA e 5-CQA), cafeína, trigonelina, fenóis e sacarose, mostram ter estreita relação com a qualidade sensorial da bebida e sua classificação (FARAH et al., 2006; FRANCA et al., 2005; SILVA et al., 2005).
Outra característica bioquímica do grão que apresenta correlação com a qualidade final do café é a atividade da enzima cúprica polifenoloxidase, pois de acordo com vários autores, esta se mostra diretamente relacionada à qualidade sensorial da bebida (CARVALHO et al., 1994; MAZZAFERA et al., 2002; SILVA et al., 2009).
Segundo Carvalho et al. (1994), cafés de melhor qualidade de bebida possuem elevada atividade enzimática da polifenoloxidase e elevado índice de coloração. Esses mesmos autores verificaram que as variações da atividade enzimática da polifenoloxidase, permitem separar as classes de bebida, mostrando para o café “riado e rio” atividades inferiores a 55,99 U g-1 de amostra; nos cafés de bebida “dura” atividades entre 55,99 e 62,99 U g-1 de amostra; nos cafés de bebida “mole” atividades entre 62,99 e 67,66 U g-1 de amostra e nos cafés de bebida “estritamente mole” atividades superiores a 67,66 U g-1 de amostra, constatando assim um aumento significativo na atividade da polifenoloxidase à medida que o café se apresenta com melhor qualidade.
Dentre as condições de manejo, a adubação e a nutrição da planta podem influenciar a composição química do grão, o qual, após torrado, produz compostos que conferem características de aroma e sabor ao café. Essa influencia da nutrição mineral foi verificada em vários trabalhos de pesquisa para nitrogênio e potássio (SILVA et al., 1999, SILVA et al., 2002; MALTA et al.,2003; CLEMENTE, 2010).
Em relação aos micronutrientes e sua influencia na formação de compostos nos grãos e na qualidade da bebida do café, poucos são os estudos, limitando-se ao efeito do Zn na qualidade da bebida do café (POLTRONIERI et al. 2011; MARTINEZ et al. 2013).
Mediante o exposto, e em virtude da busca pela produção de cafés de melhor qualidade percebe-se a necessidade de se pesquisar a relação da nutrição mineral com micronutrientes com a qualidade da bebida do café, entre os quais o Zn. O Zn está ligado ao metabolismo do nitrogênio nas plantas e atua na síntese de aminoácidos, carboidratos e síntese de proteínas, um dos principais componentes de membranas (proteínas periféricas e integrais) (PRADO, 2008; MENGEL e KIRBY, 2001).
Contudo, são poucos os relatos sobre a relação entre o Zn com a qualidade dos grãos de café, Poltronieri et al. (2011) e Martinez et al. (2013) verificaram que esse micronutriente, independentemente da forma de fornecimento, influencia positivamente a produção e a qualidade de grãos de café, caracterizada pela condutividade elétrica e o potássio lixiviado dos grãos.
No contexto destas considerações, este estudo teve como objetivo avaliar a influência do Zn sobre composição química dos grãos de café, qualidade da bebida e produção de grãos.
MATERIAL E MÉTODOS
Sistema de cultivo e condução do experimento
O experimento foi conduzido em casa de vegetação do Departamento de Fitotecnia da Universidade Federal de Viçosa (UFV), situada no município de Viçosa, MG, localizada nas coordenadas 20º 45’S sul e 42º 51’O, com altitude média de 651 m, no período de agosto de 2010 a agosto de 2013. A temperatura média anual durante o período de condução do experimento foi de 22,4 ºC, com temperatura máxima de 45 ºC e mínima de 12 ºC, dentro da casa de vegetação.
O delineamento experimental utilizado foi o inteiramente casualizado com três repetições, sendo cada parcela constituída por 2 vasos, contendo cada um, uma planta, totalizando 72 vasos.
Os tratamentos consistiram de doses de Zn em solução nutritiva. No primeiro ano de avaliação empregaram-se as doses de 0,5; 1,0; 2,0; 3,0 e 4,0 µmol L-1de Zn. No segundo ano de avaliação as doses foram ajustadas para 0,2; 1,0; 2,0; 3,0 e 4,0 µmol L-1 de Zn. A mudança na dose de Zn foi feita em virtude das plantas mostrarem alta produção na menor dose e nas demais doses apresentarem toxidez, ou seja, redução na produção, com isso reduziu-se o valor da dose para poder-se encontrar o ponto de mínimo com a menor dose. Nos dois anos houve um tratamento adicional em que se forneceu 0,5 µmol L-1 de Zn via solução nutritiva, mais pulverizações foliares mensais, à base de sulfato de Zn nas concentrações de 0,2%, sendo aplicado um total de 12 pulverizações a cada ano de cultivo. Os demais nutrientes foram fornecidos nas concentrações preconizadas por Clemente et al (2013).
Foram utilizadas mudas enxertadas em fenda cheia, de café da variedade Catuaí Vermelho IAC 99. Foi utilizada a própria variedade IAC 99 como porta enxerto (cavalo) e enxerto (cavaleiro). Para o enxerto foram utilizados somente os ramos plagiotrópicos. O processo de enxertia foi feito com intuito de reduzir a fase vegetativa das plantas, favorecendo com isso uma frutificação precoce. Na fase pré-experimental as plantas foram conduzidas em recipientes retangulares de polietileno rígido (30 cm x 74 cm x 14 cm), com volume de 25 litros com solução nutritiva de 0,5 força e aeração forçada.
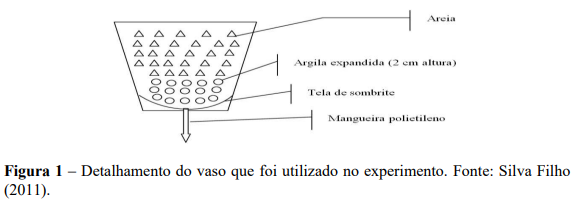
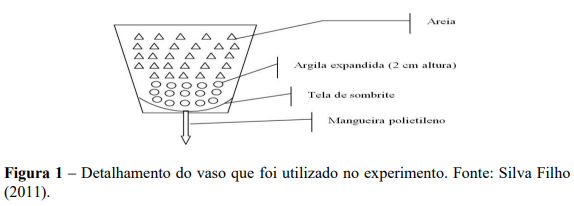
Posteriormente as mudas foram transplantadas para os vasos plásticos com capacidade de 11 L, contendo uma muda por vaso, preenchidos com areia lavada e uma camada de 2 cm de argila expandida no fundo recoberta por tela de sombrite de 50%, conforme Figura 1. No segundo ano de condução as plantas foram transferidas para vasos de 20 L de capacidade preparados da mesma forma descrita anteriormente. Os substratos (areia e argila expandida) utilizados, foram lavados com HCl a 18% e ácido oxálico a 1%, água e água desionizada conforme descrito por Martinez e Clemente (2011).
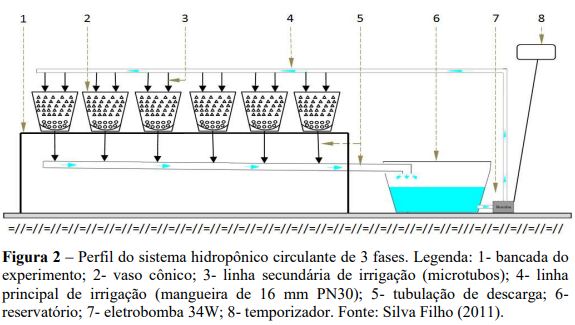
O sistema hidropônico utilizado foi o de três fases circulante. As plantas receberam diariamente aplicações de solução nutritiva no volume de 9,6 litros/vaso, cujo excesso foi drenado para um reservatório de descarga de 50 L. Esse reservatório foi equipado com eletrobomba que recalcava a solução drenada para os vasos, conforme a Figura 2. O controle da circulação da solução nutritiva foi realizado com o auxilio de um temporizador analógico programado para acionar a eletrobomba durante 1 minuto com vazão de 1,6 L/min por vaso e intervalos de 3 horas entre irrigações durante o dia. À noite o sistema permanecia desligado.
A solução nutritiva continha 6; 0,5; 3,23; 2,25; 1 e 1,75 mmol L-1 de N, P, K, Ca, Mg, S e 40; 12; 23; 0,5 e 0,3 µmol L-1 de Fe, Mn, B, Cu e Mo, respectivamente, conforme descrito por Clemente et al (2013). O volume da solução foi monitorado diariamente, e completado com água até o volume inicial de 50 L em cada reservatório. O pH da solução foi monitorado e mantido entre 5,5 e 6,0 mediante ajustes com a adição de HCl ou NaOH. Para determinar o momento da troca da solução nutritiva foram utilizados os valores de condutividade elétrica (CE), procedendo-se a troca ao verificar-se uma depleção correspondente a 30% da CE inicial. Foram utilizados os seguintes sais: KH2PO4, MgSO4, K2SO4, KNO3, Ca(NO3)2, NaNO3, CuSO4, ZnSO4, MnCl2, H3BO3, (NH4)6Mo7, FeCl2 e Na2EDTA.
A solução nutritiva foi contida em 12 reservatórios de plástico de 50 L, segundo os tratamentos e cada reservatório forneceu solução a seis vasos com uma planta cada. As soluções estoque de macronutrientes foram purificadas pelo método da APDC (amoniopirrolidinaditiocarbamato) e a solução de FeCl3 usando-se a resina trocadora especifica para Zn (Dowex 1X-8 de 50 mesh) conforme descrito por Martinez e Clemente (2011).
Avaliações
a) Produção
Os frutos foram colhidos individualmente no estádio de maturação cereja. Foram avaliadas as produções das duas plantas da parcela, sendo feita a contagem dos frutos de cada planta, sendo esse valor convertido em produção por planta (frutos/planta).
Posteriormente os frutos foram colocados para secar sobre leito de papel toalha, sobre bancadas, em casa de vegetação até atingirem 11 a 12% de umidade. Após a secagem, foram descascados obtendo-se assim os grãos beneficiados. Os grãos beneficiados foram pesados, obtendo-se o peso das duas plantas da parcela, sendo esse valor convertido em produção por planta (g/planta), e posteriormente foram feitas as análises químicas.
b) Estado nutricional das plantas
O estado nutricional das plantas foi avaliado no início do pleno florescimento da cultura. Para realizar análise química foliar foram coletadas as folhas do terceiro ou quarto nó, contado do ápice para a base, dos ramos plagiotrópicos em floração. O material amostrado foi lavado em água desionizada e seco em estufa de ventilação forçada de ar a 70 ºC, por 72 horas. Em seguida o material foi moído em moinho tipo Wiley equipado com peneira de 20 mesh. Os teores de Zn foram determinados por espectrofotometria de absorção atômica conforme método adaptado de Malavolta et al. (1997).
c) Qualidade dos Grãos
Acidez titulável
A acidez titulável foi determinada pelo método descrito pela AOAC (1990). Amostras de 1 g de café cru moído receberam 25 mL de água destilada e foram colocadas em agitador elétrico por 1 hora a 150 rpm, em seguida procedeu-se a filtragem em papel de filtro. Uma alíquota de 5 mL da solução filtrada foi adicionada a um erlenmeyer junto a 50 mL de água destilada e 3 gotas de fenolftaleína (1%), procedendo-se a titulação com NaOH (0,1 mol L-1). O resultado foi expresso em mL de NaOH 0,1 (mol/L)/100g de amostra.
Ácidos orgânicos
Os ácidos orgânicos (málico, tartárico e cítrico) foram determinados de acordo com Scherer et al., (2012). Uma amostra de 0,3 g, de grãos de café moído foi triturada em politron com 10 mL de água ultra-pura. Uma alíquota de 0,5 mL foi agitada com 1,5 mL da fase móvel que constiuiu-se de KH2PO4 0,01 mol L-1 (pH 2,6). O sobrenadante foi filtrado em filtro com membrana de 0,45 μm, e injetado diretamente em tubos de HPLC. As análises foram realizadas por cromatografia líquida de alta eficiência (CLAE), com coluna C18 de fase reversa.
Potencial hidrogeniônico (pH)
O pH foi determinado pelo método descrito pela AOAC (1990). Amostras de 2g de café cru moído receberam 50 mL de água destilada e foram colocadas em centrifuga por 1 hora a 150 rpm. Em seguida foi feita a filtragem em papel de filtro quantitativo de 9 cm de diâmetro e posteriormente foi feita a leitura com peagâmetro digital.
Fenóis Totais
A determinação dos compostos fenólicos totais na bebida do café foi realizada pelo método de Folin Denis, descrito pela Association of Official Agriculture ChemistsAOAC (1990). Uma amostra de 0,5 g de grãos foi extraída com 30 mL de metanol 50% sob agitação constante durante 15 minutos usando-se tubos com tampa rosqueada, seguido de filtragem em papel de filtro qualitativo no 4.
Em uma alíquota de 0,1 mL do extrato adicionaram-se 2,5 mL de uma solução aquosa do reativo de Folin-Ciocalteu (10%) e 2,0 mL de uma solução recém-preparada de carbonato de sódio a 7,5%. Manteve-se solução em um banho de água a uma temperatura de 50 ºC por 5 minutos. A absorbância foi registrada em um espectrofotômetro de UV/VIS a 760 nm. A curva de calibração foi feita com solução aquosa de ácido gálico nas concentrações de 10, 20, 30, 40 e 50 μg mL-1. As leituras foram feitas contra um branco. Os resultados foram expressos em equivalentes de ácido gálico.
Ácidos clorogênicos (3- cafeoilquinico, 4-cafeoilquinico e 5-cafeoilquinico)
Os ácidos clorogênicos foram extraídas com metanol aquoso (40 %) e clarificado com soluções de Carrez I e II (FARAH et al, 2005; TRUGO e MACRAE, 1984). As extrações foram realizadas da seguinte forma: amostras de café moído (0,5 g) foram extraídas com 80 mL de metanol 40% e transferidas para balões volumétricos de 100 mL. Em cada amostra foram adicionados 2 mL das soluções Carrez 1 e 2; após completar o volume para 100 mL e agitar, a mistura foi deixada em repouso por 10 minutos. O preciptado foi filtrado em papel de filtro Watman n0 1; posteriormente foi passado novamente em filtro com membrana de 0,45 μm, e injetado diretamente em tubos de HPLC. A curva de calibração foi plotada usando-se a mistura de isômeros em concentrações variando de 10 a 100 μg mL-1 .
Polifenoloxidase (PPO)
Uma amostra de 1 grama de café cru foi moído e colocada com 10 mL de tampão fosfato de sódio 0,1 mol L-1, pH 6b, a 40C, contendo 1% de ácido ascórbico. O material foi deixado em banho de gelo sob agitação por 10 minutos. Em seguida o extrato foi filtrado em papel de filtro comum, e o filtrado mantido em gelo para posterior dosagem da atividade.
O substrato utilizado para a dosagem da atividade da enzima foi o DOPA (3,4 – dihidroxifenilalanina), como usado por Carvalho et al. (1994) e Correa et al. (1997) – 8 mg de DOPA dissolvidos em 10 mL do tampão fosfato 0,1 mol L-1, pH 6,0.
A seguir, em uma alíquota de 900 μL do tampão fosfato 0,1 mol L-1, pH 6.0 contendo DOPA foram adicionados 100 μL do extrato. Imediatamente após a adição do extrato na cubeta de leitura foi feita a leitura de absorbância em 420 nm, e a partir daí a cada 15 segundos durante 5 minutos.
Índice de coloração
O índice de coloração foi determinado pelo método descrito por Singleton (1966), adaptado para café. Uma amostra de 1 g de café cru moído foi colocado em erlenmeyer ao qual foram adicionados 25 mL de água destilada. A amostra foi homogeneizada em agitador por 1 hora. Procedeu-se a filtragem em papel de filtro quantitativo de 9 cm de diâmetro, sendo tomada uma alíquota de 5 mL do filtrado aos quais foram adicionados a 10 mL de água destilada. As amostras foram deixadas em repouso por 20 minutos e lidas em espectrofotômetro ajustado para 425 nm.
Cafeína e trigonelina
Os componentes químicos cafeína e trigonelina foram determinados pelo método descrito por Mazzafera (1994) e Vitorino et al. (2001). Os grãos de café foram moídos em moinho de bolas e uma amostra de 0,1 g foi extraída com 10 mL de metanol 80% durante 1 hora em banho-maria (80 0C), com ocasional agitação. Depois de resfriarem em temperatura ambiente, uma alíquota de 2 mL foi centrifugada em durante 10 minutos. O sobrenadante foi filtrado em filtro com membrana de 0,45 μm, e injetado diretamente em tubos de HPLC. As análises foram realizadas por cromatografia líquida de alta eficiência (CLAE), com coluna Acclaim 120 C18 de fase reversa. O sistema encontrava‑se acoplado a um fotodetector de arranjo de diodos que por sua vez estava conectado por interface a um microcomputador para processamento de dados.
A análise de cafeína foram feitas tendo como solvente o metanol e água na proporção de 40:60 e fluxo de 1 mL minuto-1, sendo detectada em 272 nm. A quantificação foi feita por comparação com o padrão de cafeína pura.
As análises de trigonelina foram feitas tendo metanol, água e ácido acético na proporção de 20:79:1 e fluxo de 1 mL minuto-1, sendo detectada em 265 nm. A quantificação foi feita por comparação ao padrão externo de trigonelina pura. A curva de calibração para cafeína e trigonelina foi feita em concentrações variando de 0 a 175 μg mL-1 .
Proantocianidinas
Uma amostra de 0,3 g de café moído foi extraído com 10 mL de metanol 80% sob agitação constante durante 24 horas em temperatura ambiente, usando-se tubos com tampa rosqueada, seguido de filtragem em papel de filtro qualitativo no 4.
Transferiu-se 0,10 mL do extrato bruto para um tubo de ensaio e adicionaram-se 2,0 ml de uma solução recém preparada de vanilina em ácido sulfúrico 70% na concentração de 1g/100mL. A solução resultante foi colocada em banho de água a 50 ºC por 15 minutos. Mediu-se a absorbância a 500 nm. Juntamente com os extratos preparou-se uma curva de calibração com catequina nas concentrações de 2, 5, 10, 20 e 30 μg mL-1. Tanto as amostras quanto os padrões da curva de calibração passaram pelo mesmo tratamento. A leitura foi feita contra um branco e os resultados expressos em equivalentes de catequina (HAGERMAN, 2002 e HASLAM, 1989).
Sacarose
Uma amostra de 0,05 g foi colocada em tubo de centrífuga, na qual foi adicionado 1 mL de etanol 80%, em seguida foram imersos em banho de água (80 0C) durante 20 minutos. Posteriormente as amostras foram centrifugadas e o sobrenadante vertido em outro tubo de centrífuga. Sobre o resíduo foi adicionado 1 mL de etanol 80% e o processo foi repetido novamente. Os sobrenadantes foram centrifugados durante 1 minuto, passado em filtro de membrana de 0,45μm e injetado em tubos de HPLC.
Para determinação da sacarose foi utilizado um detector de índice de refração e uma coluna SP 0810 (300mm X 8 mm) em temperatura de 80 0C; utilizou-se água ultrapura como fase móvel em fluxo de 1 mL/minuto. A curva de calibração foi feita nas concentrações de 0; 0,5; 1,0 e 1,5 mg mL-1 utilizando-se sacarose pura (SLUITER et al. 2008).
Glicose, manose, arabinose e galactose
Os açucares redutores (glicose, manose, arabinose e galactose) foram determinados pelo método descrito por SLUITER et al., (2008). Amostras de café (0,5 g) foram submetidas à hidrólise ácida com 3 mL de ácido sulfúrico 72% e mantidas em banho-maria (50 0C) durante 7 minutos. Posteriormente ao pré-tratamento foram adicionados 84 mL de água ultra-pura, as amostras foram autoclavadas durante 45 minutos (121 0C). Depois de resfriadas a temperatura ambiente, uma alíquota de 10 ml foi transferida para enlenmeyer e o pH corrigido para valores entre 4 e 6 com carbonato de cálcio puro. O sobrenadante foi coletado e passado em membrana de filtro de 0,45 μm e injetados em tubos para HPLC.
Para determinação desses açúcares foi utilizado um detector de índice de refração a 50 0C e uma coluna SP 0810 (300mm X 8 mm) em temperatura 80 0C; utilizou-se água ultra-pura como fase móvel e fluxo de 0,6 mL minuto-1. A quantificação foi feita por comparação com os padrões de glicose, manose, arabinose e galactose. A curva de calibração foi construída nas concentrações de 0,1; 0,5; 1,0; 1,5; 2,0 e 2,5 mg ml-1 para todos os açúcares.
Potássio lixiviado e condutividade elétrica
O potássio lixiviado e condutividade elétrica foram determinados pelo método descrito por Prete (1992). Amostras de 50 grãos de café beneficiado foram colocadas em copos plásticos de 180 mL, aos quais foram adicionados 75 mL de água destilada; em seguida foram colocadas em estufa ventilada por 5 horas. Após esse tempo foram realizadas leituras das condutividades eletricas. De cada amostra retirou-se uma alíquota para realizar a leitura do K lixiviado em fotômetro de chama.
Teor de água
O teor de água foi determinado pelo método padrão da estufa a 105±1ºC por 24 horas, de acordo com metodologia proposta por Mara (1992).
Análise sensorial
A prova de xícara foi realizada no segundo ano de produção, por provadores profissionais da “3 Irmãos Corretora de Café”. Para realização das análises estatísticas os resultados obtidos para classificação da bebida pela prova de xícara foram convertidos em valores numéricos. Estes valores constam na tabela 1.

d) Análise estatística
Os dados obtidos foram submetidos à análise de variância (ANOVA) e regressão. Aplicou-se análise de regressão para avaliar os efeitos de doses de Zn e teste de Dunnett para comparar as doses de Zn com o tratamento testemunha. Os modelos foram selecionados com base na significância, dos coeficientes de regressão utilizando-se o teste “t”, adotando-se o nível de 5% de probabilidade, no fenômeno biológico e no coeficiente de determinação. Os dados foram analisados usando-se o programa SAEG 9.0 (Sistema de Análise Estatística e Genética) (SAEG, 2007).
RESULTADOS E DISCUSSÃO
a) Produção
No primeiro e no segundo anos de produção do cafeeiro, houve redução linear na produção média de grãos por planta com o aumento das doses de zinco na solução nutritiva, com menor produção na maior dose de Zn de 4,0 µmol L-1 (Figuras 3A e 3B). No primeiro ano de produção os teores foliares corresponderam na maior dose de Zn a 10,9 mg kg-1 ( Υ 5,4521 1,3667Zn; ˆ r 2 0,69), no segundo ano a de 12,76 mg kg-1 de Zn ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ). No primeiro ano a dose de 0,5 µmol L-1 de Zn, proporcionou a maior produção de frutos (12 g/planta) e no segundo ano na dose de 0,2 µmol L-1 de Zn, verificou-se a maior produção de frutos (103 g/planta), com teor foliar de 6,13 e 10,63 mg kg-1 de Zn respectivamente.
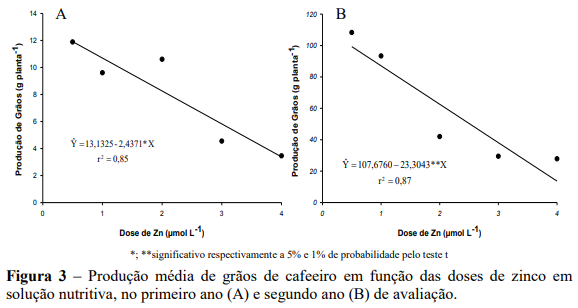
Foi constatado que elevados teores de zinco em plantas de cafeeiro, reduzem a expansão foliar, o que indica toxidez do zinco, sendo a produção de frutos a característica mais afetada pelo zinco, principalmente sob teores elevados. Pode-se atribuir também a queda na produção de frutos a uma menor disponibilidade de fotoassimilados para esses órgãos nas plantas, pois em folhas maduras com elevados teores de zinco a produção de fotoassimilados é normal, mas a sua exportação para as regiões de consumo é inibida (FAVARO, 1992).
Sagardoy et al., (2009) trabalhando com plantas de beterraba em solução nutritiva com elevadas doses de zinco, verificaram redução na fotossíntese das plantas, com o esgotamento de CO2 no sitio de carboxilação da Rubisco, reduções drásticas na condutância estomática (70%) e na condutância do mesofilo (44%).
A redução na produção de frutos pode estar relacionada também com interações negativas entre os outros cátions e o zinco, em que o excesso de zinco pode provocar deficiência induzida, de Fe, Cu e Mn devido aos raios iônicos semelhantes (BOARDMAN e MCGUIRE, 1990; SAGARDOY et al, 2009).
Estão na Tabela 2, os valores médios de frutos por plantas (FP), produção de grãos, massa de 100 grãos (MAS100G) e dos frutos de café em coco obtidos com doses de Zn e o tratamento que recebeu pulverizações foliares mensais com Zn (Testemunha). Nota-se que o número de frutos por plantas (FP) e peso dos grãos nas doses de Zn de 2,0; 3,0 e 4,0 µmol L-1 foram inferiores aos da testemunha, tendo a testemunha apresentado valores superiores de número de frutos em 44%, 71% e 81% e de peso dos grãos de 51%, 77% e 82% comparativamente as doses 2,0; 3,0 e 4,0 µmol L-1 de Zn (Tabela 2). Já para a massa de 100 grãos (MAS100G) e dos frutos de café em coco todas as doses de Zn (0,5; 1,0; 2,0; 3,0 e 4,0 µmol L-1) apresentaram resultados inferiores aos da testemunha.
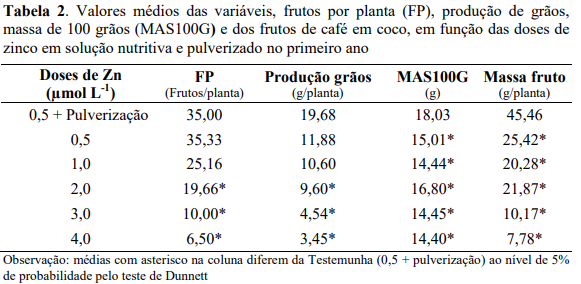
O aumento das doses de Zn na solução nutritiva promoveu redução no número e na produção dos frutos de café. Este efeito pode estar relacionado à toxidez provocada pelo excesso de zinco, pois segundo Khurana e Chatterjee (2001), o excesso de Zn provoca diminuição significativa, da biomassa, da concentração de clorofila (a, b) e proteínas solúveis nas plantas.
b) Qualidade dos Grãos
Acidez titulável
Nos dois anos de avaliações observou-se efeito quadrático das doses de Zn na acidez titulável (AT), em que a acidez decresceu até um ponto de mínima e, posteriormente, aumentou com o incremento das doses de Zn. No primeiro ano a menor acidez titulável (48,37 mL NaOH 100 g-1) foi verificada na dose estimada de 2,68 µmol L -1 e teor foliar de Zn de 8,20 mg kg-1 (Υ 5,4521 1,3667Zn; ˆ r 2 0,69), já para maior dose de zinco verificou-se um aumento na AT correspondendo ao valor de 49,42 mL NaOH 100 g-1 (Figura 4A). No segundo ano a menor acidez titulável foi verificada na dose estimada de 2,16 µmol L-1, correspondendo a acidez titulável de 114,87 mL NaOH 100 g-1 e teor foliar de Zn de 9,92 mg kg-1 ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ), enquanto que a para maior dose de zinco verificou-se um incremento na AT correspondendo ao valor de 137,49 mL NaOH 100 g-1 (Figura 4b).
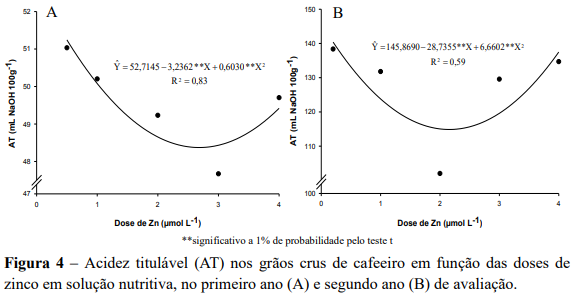
Comparando os valores estimados de acidez titulável, (Figura 4A e 4B), com os encontrados por Carvalho et al. (1994), pode-se observar que, apesar de ter ocorrido diferença significativa nas doses de Zn, o menor e o maior valor da acidez titulável encontrado no primeiro ano (48,37 e 49,42 mL NaOH 100 g-1) e no segundo ano (115,57 e 137,49 mL NaOH 100 g-1), estão abaixo da faixa de classificação como café de bebida dura, riada e rio (250,4; 272,2 e 284,5 mL de NaOH 0,1N 100 g-1), ou seja, apesar de ter ocorrido efeito das doses de Zn a influencia na qualidade dos grãos de café quanto a AT é pequena comparativamente a outros fatores. No presente trabalho a qualidade do café se enquadra em cafés especiais, pelos baixos valores de acidez.
De acordo com Carvalho et al. (1994), a AT dos grãos de café tem uma relação inversa com a qualidade da bebida do café, pois cafés de melhor qualidade possuem maior atividade enzimática da polifenoloxidase e índice de coloração e, menor acidez titulável total. Os mesmos autores ressaltam a importância da utilização da acidez titulável total em conjunto com a atividade da polifenoloxidase e índice de coloração como suporte, para uma maior eficiência da classificação sensorial da bebida do café.
Ácidos orgânicos
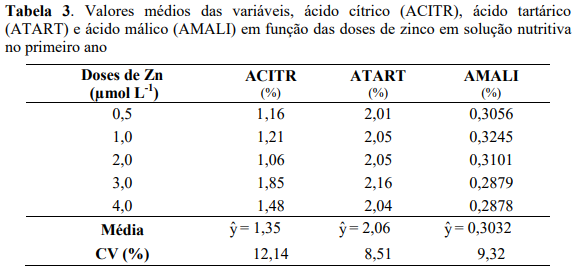
Na Tabela 3 são mostrados os valores médios, do primeiro ano de avaliação, dos teores de ácidos cítricos, tartárico e málico nos grãos de café em função das doses de zinco via solução nutritiva. Não houve diferença significativa desses teores em função das doses de zinco em solução nutritiva, como também não houve uma tendência definida de variações desses ácidos.
No segundo ano de avaliação os resultados (Figuras 5A, 5B e 5C) demonstram que as doses de Zn via solução nutritiva influenciaram significativamente os teores dos ácidos cítricos, tartárico e málico. Para o ácido cítrico verifica-se resposta quadrática, que apresentou na dose estimada de 0,94 µmol L-1 de Zn o maior teor de acido cítrico correspondente a 1,20% e com teor foliar de 9,92 mg kg-1 de Zn ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ). Com o incremento das doses de Zn houve redução nos teores, atingindo na maior dose de Zn (4,0 µmol L-1) o menor teor do ácido (0,95%), isso corresponde a uma redução de 21% em comparação ao valor máximo(Figura 5A).
Resultado semelhante foi observado para os teores do ácido tartárico, apresentando na dose estimada de 1,50 µmol L-1 de Zn os maiores valores correspondentes a 2,56% e teor foliar de Zn de 9,73 mg kg-1 ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ), mas com o incremento das doses de Zn (4,0 µmol L-1) os teores decresceram para 1,99%, correspondendo a uma redução de 22% nos teores do ácido tartárico (Figura 3B). Para o ácido málico, verificou-se redução linear com o incremento das doses de Zn, apresentando na maior dose (4,0 µmol L-1) o menor teor, correspondente a 0,22%, e teor foliar de Zn de 12,75 mg kg-1 ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ), correspondendo a uma redução de 22% nos teores do ácido málico em comparação à menor dose de Zn que proporcionou teores de 0,35%.
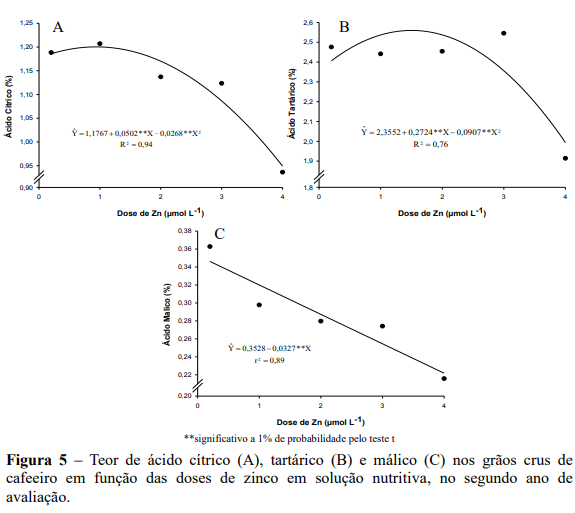
Esses ácidos são originários de diversas rotas bioquímicas, bem como da fermentação dos açúcares por microorganismos existentes na polpa e na mucilagem dos frutos (CHALFOUN, 1996).
Na tabela 4, são apresentadas as comparações entre os valores de pH, teores dos ácidos cítricos, tartárico, málico e a acidez total titulável obtidos com as diferentes doses de Zn fornecidas via solução nutritiva e o tratamento testemunha, que recebeu o nutriente via foliar. Os resultados demostram que houve diferença significativa somente para ácido cítrico e acidez titulável, em que os teores do ácido cítrico da testemunha foram inferiores ao da dose de 3,0 µmol L-1 e não diferiram das demais doses, enquanto que para a acidez titulável houve diferença significativa da testemunha em relação às doses de 0,5 e 3,0 µmol L-1, em que os valores de acidez titulável da testemunha foram inferiores aos da menor dose de Zn (0,5 µmol L-1) e superiores aos da maior dose de 3,0 µmol L-1, demonstrando com isso que doses mais altas de zinco podem influenciar positivamente aspectos da qualidade da bebida tanto via pulverização foliar como via sistema radicular.
No entanto para as demais características como, pH, ácido tartárico e málico não houve diferença da testemunha pulverizada em comparação as doses de Zn fornecidas somente via solução nutritiva.
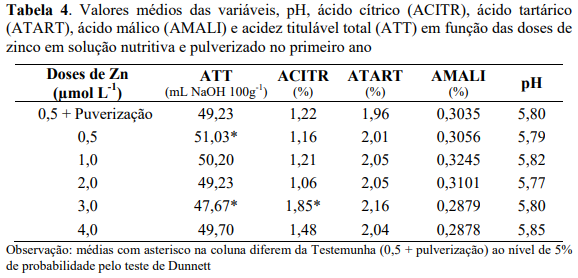
Potencial hidrogeniônico (pH)
Em relação aos valores de pH, observou-se efeito significativo das doses de zinco, somente no primeiro ano, verificando-se na dose estimada de 1,85 µmol L-1 de Zn, o menor valor de pH de 5,78, e com teor foliar de 7,98 mg kg-1 de Zn ( Υ 5,4521 1,3667Zn; ˆ r 2 0,69). Enquanto para maior dose de Zn de 4,0 µmol L-1 o maior valor do pH foi 5,86 (Figura 6). Para o segundo ano não houve ajuste de regressão para os valores de pH. De acordo com Pinto et al., 2002 em grãos de café torrado, as bebidas estritamente mole, mole e riada - apresentaram menores valores de pH (5,30 a 5,32) comparativamente as bebidas rio e rio-zona.
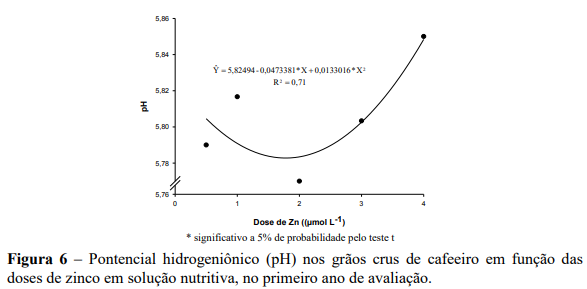
Fenóis Totais
Nos dois anos de avaliação observou-se efeito de raiz quadrático das doses de Zn nos teores de fenóis totais, em que os teores de fenóis totais decresceram até um ponto de mínima e, posteriormente, aumentou com o incremento das doses de Zn (Figura 7).
No primeiro ano o menor teor de fenóis foi de 5,07% na dose estimada de 1,85 µmol L-1, correspondendo ao teor foliar de 7,98 mg kg-1 ( Υ 5,4521 1,3667Zn; ˆ r 2 0,69). Na maior dose de zinco verificou-se um maior teor de fenóis correspondendo ao valor de 6,2% (Figura 7A). No segundo ano o menor teor de fenóis (6,49%), foi verificado na dose estimada de 1,55 µmol L-1, com teor foliar de 9,73 mg kg-1 ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ), enquanto que a para maior dose de zinco verificou-se um maior teor de fenóis correspondendo ao valor de 7,33% (Figura 7B).
A menor produção de fenóis ocorreu com doses de Zn variando entre 1,55 e 1,85 e µmol L-1 as quais resultaram em plantas com teores foliares entre 7,98 e 9,73 mg kg-1, ou seja, plantas com nutrição adequada, segundo as faixas críticas estabelecidas por Martinez et al. 2003. Doses menores ou maiores de Zn resultaram em maior produção de fenóis. No caso de doses elevadas de Zn, pode-se supor que interações entre o Cu e o Zn, cujos raios iônicos são semelhantes, possam ter provocado deficiência induzida de Cu, elevando a produção de fenóis (BOARDMAN; MCGUIRE, 1990; SAGARDOY et al, 2009).
Ácidos clorogênicos (3- cafeoilquinico, 4-cafeoilquinico e 5-cafeoilquinico)
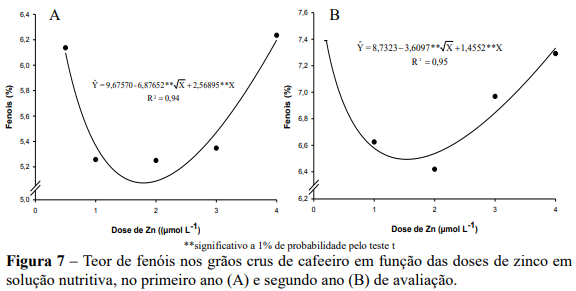
Nos dois anos de avaliações as doses de Zn influenciaram os teores do ácido 5- cafeoilquínico (5-CQA). No primeiro ano os teores do 5-CQA decresceram e, posteriormente, aumentaram apresentando na dose estimada de 1,85 µmol L-1 de Zn, o menor teor (0,92%) e teor foliar de Zn correspondendo a 7,98 mg kg-1 ( Υ 5,4521 1,3667Zn; ˆ r 2 0,69), para a maior dose de zinco verificou-se um incremento nos teores correspondendo ao valor de 1,4% (Figura 8A). No segundo ano o menor teor (1,09%) foi verificado na dose estimada de 1,94 µmol L-1, com teor foliar de Zn de 9,81 mg kg-1 ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ), na maior dose verificou-se um incremento nos teores atingindo o valor de 1,52% (Figura 8B).
Essa redução nos teores do 5-CQA com o aumento das doses de Zn, esta inversamente proporcional à atividade da PPO (Figura 9), em que à medida que os teores do 5-CQA decrescem ou aumentam, o inverso ocorre com a PPO. De acordo com Carvalho et al.(1989), existem indícios da ocorrência de maior concentração de polifenóis, como o caso do ácidos clorogênicos (CGA), em cafés de pior qualidade. Farah (2004) encontrou os maiores teores de 5-CQA em cafés com qualidade de bebida inferior.
Para os teores do ácido 4-cafeoilquínico (4-CQA) e 3-cafeoilquínico só houve efeito significativo das doses de zinco no segundo ano de cultivo (Figura 8C e Tabela 5). No segundo ano os teores do 4-CQA se ajustaram ao modelo raiz quadrática, com o menor teor (0,77%) verificado na dose estimada de 1,90 µmol L-1, e teor foliar de Zn de 9,80 mg kg-1 ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ) (Figura 6C). Quanto ao 3-CQA o efeito foi quadrático, com o maior teor (1,0%) verificado na dose estimada de 2,20 µmol L-1 de Zn, e teor foliar de Zn de 9,95 mg kg-1 ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ) (Figura 8D). Esse resultado corresponde ao incremento de 18% no teor do ácido 3-CQA, em relação à menor dose de zinco (0,85%). Na dose máxima de Zn houve redução no teor do 3-CQA de 14% em comparação ao valor máximo estimado.
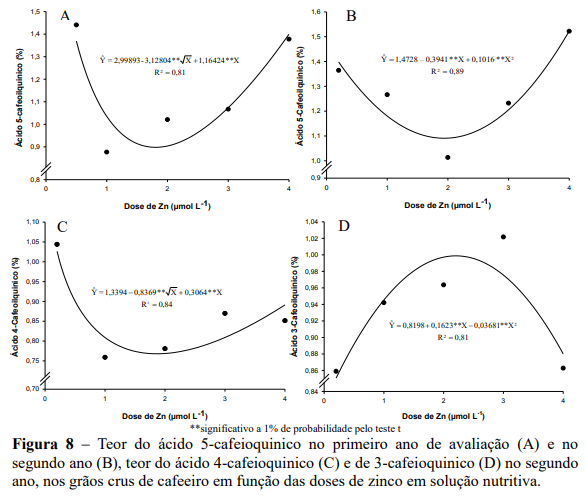
O aumento dos teores do ácido 3-cafeoilquínico varia com as doses de Zn e esta se relaciona diretamente à atividade da PPO (Figura 9), em que à medida que os teores do 3-CQA aumentam ou diminuem, ocorre o mesmo para a PPO. O inverso ocorre para os teores de fenóis totais (Figura 7). Apesar do 3-CQA ser um composto fenólico ele não segue o mesmo sentido dos demais ácidos clorogênicos (4-CQA e 5-CQA) que decresceram seus teores com o aumento das doses de Zn. (FARAH et al., 2010) observaram que ao contrário do que ocorre para os demais isômeros do ácido cafeoilquínico, maior teor de 3-CQA parece estar associado a melhor qualidade de bebida.
Segundo Farah (2009) os ácidos clorogênicos oferecem proteção em relação a estresses abióticos, tais como aqueles associados com mudanças de temperatura, disponibilidade de água, exposição a níveis de luz UV e deficiência de nutrientes minerais. Além disso, os ácidos clorogênicos contribuem para o processo de fermentação e tem uma influência marcante na determinação da qualidade de xícara do café (FARAH et al., 2006).
De acordo com Salva e Lima (2007), cafés que contêm menos ácidos clorogênicos proporcionam bebidas menos adstringentes e com sabor característico de café. Esse mesmos autores relatam que o amargor, a adstringência e o gosto de mofo da bebida de café se devem ao nível de concentração de ácidos clorogênicos e das proporções em que diferentes deles se encontram nos cafés crus. Dentre os grupos que compõe os CGAs do café, 5-CQA é o mais abundante em sementes de café.
Segundo Amorim e Silva (1968) os compostos fenólicos, principalmente os ácidos clorogênicos exercem uma ação protetora, antioxidante dos aldeídos. Os compostos fenólicos possuem alto potencial redox, sendo assim, substratos preferenciais no combate ao estresse oxidativo provocado por circunstâncias de campo, como alta intensidade luminosa, fraturas físicas, deficiências nutricionais, ataque de insetos e micro-organismos e alterações climáticas. Além da funcionalidade, contribuem expressivamente como precursores de flavor no café torrado (ARRUDA et al. 2012; LIMA et al. 2010).
No processo de torrefação os ACGs são precursores importantes dos ácidos fenólicos livres e, por conseguinte, dos compostos fenólicos voláteis que participam da formação do aroma do café processado (MOREIRA et al. 2000). Os ácidos clorogênicos reagem durante a torra, produzindo compostos ácidos, lactonas e outros derivados fenólicos que contribuem para o aroma e sabor do café, acidez final e adstringência da bebida (LÓPEZ-GALILEA et al. 2007).
Polifenoloxidase (PPO)
Nos dois anos de avaliações a atividade da polifenoloxidase (PPO) apresentou efeito quadrático em função das doses de zinco. No primeiro ano a máxima atividade da enzima foi de 82,08 U g-1 de amostra na dose estimada de 2,42 µmol L-1 de Zn, em grãos de plantas com teor foliar de 8,8 mg kg-1 de Zn ( Υ 5,4521 1,3667Zn; ˆ r 2 0,69).
Na menor e maior dose de Zn verificou-se uma menor atividade da PPO com valores de 53,75 e 63,05 U g-1 de amostra, respectivamente (Figura 9A). No segundo ano a máxima atividade da enzima foi de 85,14 U g-1 de amostra na dose estimada de 1,94 µmol L-1 de Zn, correspondendo a um teor foliar de Zn de 9,8 mg kg-1 ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ), já para menor e maior dose de Zn verificou-se uma menor atividade da PPO com valores de 68,92 e 62,31 U g-1 de amostra, respectivamente (Figura 9B).
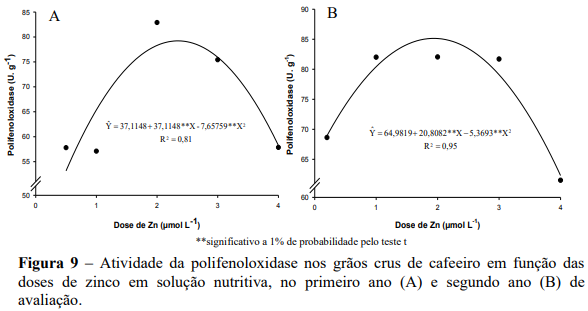
No primeiro e no segundo ano de produção, a atividade da PPO não seguiu a mesma tendência de redução da produção de grãos, verificando-se nos pontos de máxima atividade da PPO (82,08 e 85,14 U g-1 de amostra) nas doses estimadas (2,42 e 1,94 µmol L-1 de Zn), produções de grãos inferiores à produção máxima (12 g/planta e 103 g/planta), com redução de 39,67% e 39,34% na produção de grãos (7,24 g/planta no primeiro ano e 62,47 g/planta no segundo ano).
Com base na classificação proposta por Carvalho et al. (1994) em função da máxima atividade da PPO, pode-se atribuir no primeiro ano de avaliação aos grãos de café a classificação na faixa de bebida “estritamente mole”, enquanto que para a menor e maior dose de Zn os grãos de café podem ser classificados, como bebida “riado e rio” e bebida “mole” respectivamente. No segundo ano de avaliação pode-se atribuir aos grãos de café na dose de máxima atividade e na menor dose, a classificação na faixa de bebida “estritamente mole”, enquanto que para a maior dose de Zn pode-se atribuir a classificação na faixa de bebida “mole”. Segundo Carvalho et al. (1994), a polifenoloxidase esta associada diretamente com a qualidade de bebida do café, demonstrado através de sua atividade, quanto melhor a qualidade do café, maior a sua atividade enzimática.
O aumento na atividade da PPO devido à aplicação do Zn pode ser atribuído ao fato deste elemento atuar na manutenção da integridade das membranas biológicas (CAKMAK; MARSCHNER, 1990), com isso pode ter contribuído para redução de radicais livres de O2 como também na estabilização estrutural de proteínas (CAKMAK; MARSCHNER, 1988; KAYA; HIGGS, 2001). Por outro lado, observa-se, também, redução na atividade da PPO devida ao excesso de Zn. Os valores da atividade da PPO obtidos no ponto de máximo são bastante superiores aos preconizados por Carvalho et al. (1994), demonstrando com isso que o Zn exerce influência sobre a atividade da PPO e como consequência na qualidade da bebida do café.
Índice de coloração
No primeiro ano de avalição não se verificou efeito das doses de Zn sobre o índice de coloração. Para o segundo ano observou-se efeito quadrático do índice de coloração para as doses de Zn (Figura 10), apresentando na dose estimada de 2,39 µmol L-1 de Zn o maior valor do IC de 0,78 (D.O. 435 nm) e teor foliar de Zn de 10,09 mg kg-1 ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ), enquanto que para a menor e maior dose de Zn, observaram-se os menores valores do IC correspondendo a 0,42 e 0,59 (D.O. 435 nm).
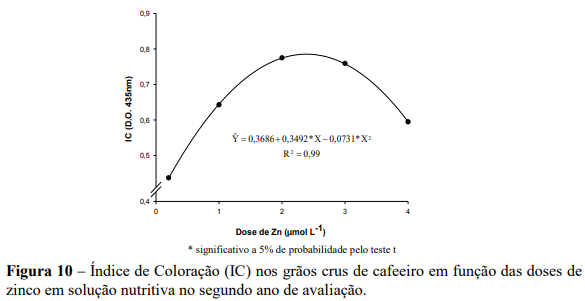
Esse resultado sugere que existe uma associação do IC com a atividade da PPO (Figura 9), pois os grãos de café com maior atividade da polifenoloxidase, apresentaram tendência de maior IC, confirmando os resultados encontrados por Carvalho et al. (1994). Cafés de melhor qualidade possuem maior atividade da PPO e IC, conforme pesquisas desenvolvidas por Carvalho et al. (1994), Leite e Carvalho (1994), Chagas et al. (1996), Silva et al. (2002) e Silva et al. (2009). Carvalho et al. (1994) estabeleceram que cafés com índices de coloração iguais ou superiores a 0,65 enquadram-se nas classes de cafés "duro", "apenas mole", "mole" e "estritamente mole". Os índices de coloração inferiores a 0,65 são classificados como "rio" e "riado", ou seja, cafés não exportáveis.
Com base na classificação proposta por Carvalho et al. (1994) em função do índice de coloração, pode-se atribuir aos grãos de café na dose de Zn correspondente ao ponto de máximo a classificação na faixa de bebida “estritamente mole”, pois os valores encontrados no presente trabalho situram-se na faixa de 0,78 (D.O. 435 nm), enquanto que para a menor e maior dose de Zn (0,42 e 0,59 D.O. 435 nm), pode-se atribuir a classificação de cafés "rio" e "riado". Para Corrêa et al. (1997) o índice de coloração possibilitou a distinção entre as bebidas dura, apenas mole, mole e estritamente mole. Porém os valores do índice de coloração encontrados por esses autores foram: 0,47, 0,54, 0,63, e 0,72 respectivamente.
Observa-se na tabela 5, que houve diferença significativa das doses de Zn fornecidas via solução nutritiva em comparação com a testemunha que recebeu pulverizações foliares, para as variáveis, 5-CQA e fenóis totais, em que o isômero do ácido clorogênico 5-CQA e os teores de fenóis totais da testemunha foram inferiores aos das doses de Zn (0,5 e 4,0 µmol L-1), enquanto que as demais doses de Zn não diferiram da testemunha.
Para as variáveis, PPO e o índice de coloração (Tabela 5), houve diferença significativa das doses de Zn fornecidas via solução em comparação com a testemunha, em que a atividade da enzima PPO da testemunha foi superior aos das doses de Zn (0,5; 1,0 e 4,0 µmol L-1) e não diferiram das demais doses.
Para o índice de coloração, houve diferença significativa somente na dose de Zn de 3,0 µmol L-1 em comparação a testemunha, em que o índice de coloração da testemunha foi inferior ao da dose de Zn (3,0 µmol L-1), tendo a testemunha apresentado índice de coloração de 1,16 DO. 435nm e a dose de Zn de 1,66 DO. 435nm.
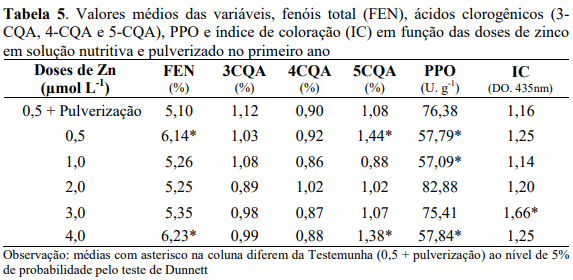
Com base na classificação proposta por Carvalho et al. (1994) em função da PPO, pode-se atribuir aos grãos de café na pulverização com Zn (Testemunha) a classificação na faixa de bebida “estritamente mole”, enquanto que para as menores e maior dose de Zn os grãos de café podem ser classificados, como bebida “dura”. Segundo Carvalho et al. (1994) grãos de café com maior atividade da polifenoloxidase, apresenta tendência de maior IC.
Cafeína e trigonelina
Nos dois anos de avaliação observou-se efeito quadrático das doses de Zn sobre os teores de cafeína. No primeiro ano verificou-se na dose estimada de 2,2 µmol L-1 de Zn, o maior teor de cafeína (1,21 g 100 g-1) (Figura 11A) e teor foliar de Zn de 8,45 mg kg-1 ( Υ 5,4521 1,3667Zn; ˆ r 2 0,69).
No segundo ano o teor máximo de cafeína (1,30 g 100 g-1) foi verificado na dose estimada de 1,96 µmol L-1 de Zn, correspondendo ao teor foliar de Zn de 10,27 mg kg-1 ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ), enquanto que nas maiores doses de Zn houve redução nos teores de cafeína correspondendo ao valor de 0,88 g 100 g-1 (Figura 11B).
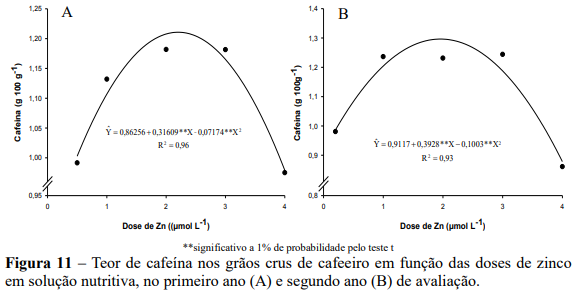
A cafeína é a principal purina na composição do café e encontra-se na polpa, no citoplasma e ligada à parede celular (MENEZES, 1990). Segundo Malta et al. (2003), esse alcalóide tem papel importante como estimulante. Segundo Illy e Viani (1995), a quantidade de cafeína presente no café é responsável por 10% de seu amargor, no entanto, o teor de cafeína não tem efeito direto na qualidade sensorial. Por outro lado, Franca, Mendonça e Oliveira, (2005) e Farah et al. (2006) encontraram maiores teores de cafeína em amostras de café arábica de alta qualidade, quando comparadas com as demais.
Nos dois anos houve efeito significativo das doses de Zn nos teores de trigonelina. No primeiro ano os teores de trigonelina se ajustaram ao modelo raiz quadrática, com o maior teor (3,64 g 100 g-1) verificado na dose estimada de 1,86 µmol L-1 de Zn, e teor foliar de Zn de 8,0 mg kg-1 ( Υ 5,4521 1,3667Zn; ˆ r 2 0,69), enquanto que para maior dose de zinco, houve redução nos teores de trigonelina (1,80 g 100 g-1) (Figura 12A).
No segundo ano os teores de trigonelina se ajustaram ao modelo quadrático, apresentando o maior teor (0,97 g 100 g-1) na dose estima de 2,55 µmol L-1 de Zn e teor foliar de Zn de 10,27 mg kg-1 ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ), enquanto que nas maiores doses de Zn houve redução nos teores de trigonelina (0,87 g 100 g-1) (Figura 12B).
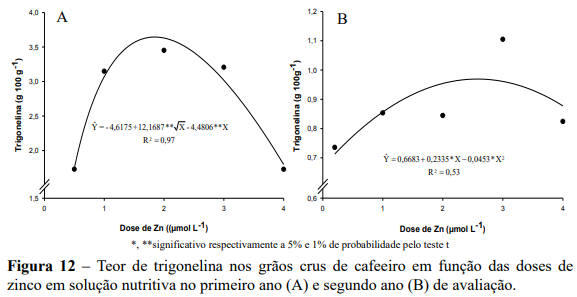
No primeiro e no segundo ano de produção, observa-se que não houve uma relação direta da produção com os teores de trigonelina, entretanto no ponto de máxima produção de trigonelina (3,64 e 0,97 g 100 g-1) nas doses estimadas (1,86 e 2,55 µmol L1 de Zn), as produções de grãos foram inferiores à produção máxima (12 g/planta e 103 g/planta), com redução de 28,33% e 53,15% na produção de grãos (8,60 g/planta no primeiro ano e 48,25 g/planta no segundo ano).
Apesar das doses de Zn terem contribuído para o aumento no teor de trigonelina nos grãos de café, os teores se apresentaram abaixo dos obtidos na dose ótima estimada na primeira safra (3,64 g 100 g-1). As doses de Zn contribuíram significativamente para o aumento no teor de trigonelina. Isso possivelmente esteja relacionado à enzima que é responsável pela formação de trigonelina via ácido nicotínico, a nicotinato Nmetiltranferase também conhecida como trigonelina sintase (KOSHIRO et al., 2006; ASHIHARA, 2006). Como o Zn está ligado ao metabolismo do nitrogênio nas plantas e atua na síntese de aminoácidos, como também na síntese protéica (PRADO, 2008), e participa diretamente ou indiretamente da ativação de varias enzimas em plantas e em diversas rotas metabólicas e bioquímicas das plantas, esse nutriente pode estar envolvidos no processo de formação da trigonelina até certo limite.
Segundo Farah et al. (2006) a trigonelina é um dos precursores do aroma do café, já que após a torra a degradação deste composto pode chegar até 90%, sendo a niacina um dos compostos formados mais conhecidos, como também a piridinas e alguns pirróis. Os mesmos autores trabalhando com amostras de cafés de diferentes qualidades, observaram que a redução da qualidade da bebida de café está associada à redução dos níveis de trigonelina nos grãos.
Proantocianidinas
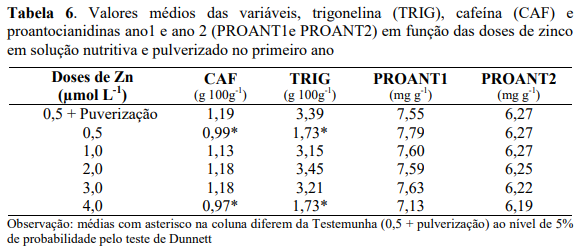
Para as proantocianidinas verificou-se uma pequena variação com o aumento das doses de Zn. No primeiro ano a variação foi de 7,13 a 7,79 mg g-1 e no segundo ano de 6,19 a 6,27 mg g-1 (Tabela 6). Nos dois anos de avaliação não houve ajuste de regressão para os teores de proantocianidinas observados. No entanto, os teores de proantocianidinas no presente trabalho no primeiro ano foram superiores e inferiores no segundo ano aos citados na literatura para o café arábica (MORAIS et al. 2009).
As proantocianidinas juntamente com os polifenóis, apresentam sabor adstringente típico, sendo um dos constituintes responsáveis pela adstringência da bebida do café (HASLAM, 1989; SILVA, 1991), interferindo com isso, no sabor e aroma do café após a torra. Observa-se na tabela 5, que houve pouca diferença significativa das doses de Zn fornecidas via solução nutritiva em comparação com a testemunha pulverizada, para as variáveis, cafeína e trigonelina, em que os teores dos dois alcaloides na testemunha foram superiores aos das doses de Zn (0,5 e 4,0 µmol L-1) e não diferiram das demais doses. As pulverizações foliares de Zn contribuíram para o aumento no teor de trigonelina e cafeína, sendo os teores obtidos para os dois alcaloides (3,39 e 1,19 g 100 g-1) respectivamente (Tabela 6). Para os teores de proantocianidinas não houve diferença significativa das doses de Zn via solução em comparação com a testemunha, demostrando com isso pouca interferência do Zn na concentração desse composto químico.
Sacarose
Nos dois anos foram observados efeitos quadráticos das doses de Zn sobre os teores de sacarose. No primeiro ano o maior teor (6,97%) foi verificado na dose estimada de 1,87 µmol L-1 de Zn e teor foliar de Zn de 8,0 mg kg-1 ( Υ 5,4521 1,3667Zn; ˆ r 2 0,69), enquanto que para dose máxima de Zn houve redução no teor de sacarose (5,09 %) (Figura 13A). No segundo ano o maior teor (8,86%) foi verificado na dose estimada de 2,14 µmol L-1 de Zn e teor foliar de 9,91 mg kg-1 ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ). Esse resultado corresponde ao incremento de 59% no teor de sacarose, em relação à menor dose de Zn, que resultou em teor de 6,24% de sacarose. Enquanto que para dose máxima de Zn houve redução de 6,43% (Figura 13B).
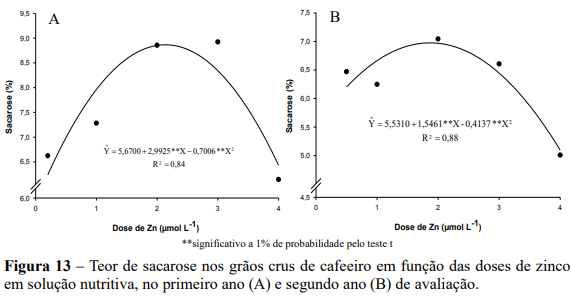
Os teores de sacarose no primeiro e segundo ano de avaliação, não seguiu a mesma tendência de redução da produção de grãos, verificando-se nos teores máximos de sacarose (6,97% e 8,86%) nas doses estimadas (1,87 e 2,14 µmol L-1 de Zn), produções de grãos inferiores à produção máxima (12 g/planta e 103 g/planta), com redução de 28,58% e 43,88% na produção de grãos (8,57 g/planta no primeiro ano e 57,80 g/planta no segundo ano).
Segundo Alloway (2004) e Mafra et al. (2004), o zinco é componente estrutural de uma gama de enzimas envolvidas em muitos processos bioquímicos, entre os quais, o metabolismo de carboidratos, fotossíntese, conversão de açúcares e metabolismo de proteínas.
Esse aumento inicial no teor de sacarose com as doses de zinco parece indicar que possivelmente esse micronutriente esteja também envolvidos na ativação da ligase da sacarose, enzima responsável pela acumulação desse açúcar em grãos de café do tipo arábico. De acordo com Alloway, (2008) são mais de 70 enzimas que contêm zinco, entre elas a aldolase, enzima envolvidas na formação da sacarose. Lantican et al., (2001) trabalhando com beterraba e milho observaram um declínio no nível de sacarose devido à menor a atividade da sintetase da sacarose. Enquanto que a redução nos teores de sacarose na maior dose de Zn, possivelmente esteja relacionada à toxidez provocada pelo excesso de Zn. A sacarose contribui com a qualidade da bebida, por ser precursora do sabor e aroma do café. Os açúcares livres dominantes nos grãos de café são, basicamente, frutose, glicose e sacarose (ROGERS et al., 1999b).
A sacarose representa quase o total dos açúcares livres nos grãos maduros de café. Em C. arabica o teor de sacarose na matéria seca varia entre 5,1 – 9,4%, no fruto maduro (CLIFFORD, 1985; KY et al., 2001; CAMPA et al., 2004; FIGUEIREDO, 2013). Segundo Franca et al. (2004), a qualidade final da bebida está intrinsecamente relacionada com a composição química dos grãos torrados.
Glicose, manose, arabinose e galactose
No primeiro ano de avaliação não houve efeito das doses de Zn sobre os teores dos açúcares redutores (manose, glicose, galactose e arabinose). No segundo ano de avaliação houve efeito significativo das doses de zinco em solução nutritiva para os teores de arabinose e manose. Com o aumento da dose de Zn via solução nutritiva, o teor de arabinose se ajustou ao modelo de raiz quadrática, com o maior teor (0,073%) verificado na dose estimada de 1,65 µmol L-1 de Zn (Figuras 14A).
O teor foliar de Zn no ponto de máxima concentração de arabinose foi de 9,74 mg kg-1 de Zn ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ). Esse resultado corresponde ao incremento de 14% no teor de arabinose, em relação a menor dose de Zn, na qual se obteve teor de 0,065%. Na dose máxima de Zn houve redução de 40% no teor de arabinose em comparação ao valor das doses que permitiram valores máximos.
Para os teores de manose observou-se incremento quadrático com o aumento das doses de Zn via solução nutritiva, com o maior teor (0,28%) verificado na dose estimada de 2,34 µmol L-1 de Zn e com teor foliar de 10,05 mg kg-1 de Zn ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ) (Figura 14B).
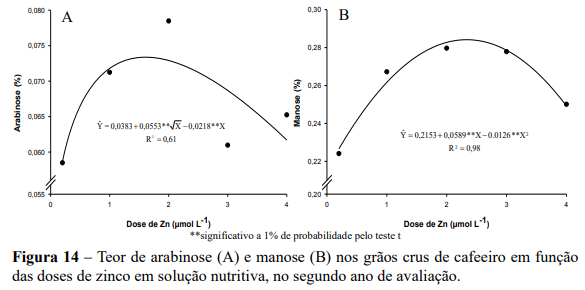
Esse resultado corresponde a incrementos de 27% e 12% no teor de manose, em relação a menor e maior dose de Zn, que resultaram respectivamente em teores de manose de 0,22% e 0,25%.
Dos açúcares solúveis presentes nos grãos de café, destacam-se a glicose, frutose, manose, galactose e a sacarose que representam uma pequena porcentagem dos carboidratos. Estes, além de atuarem como reservas de utilização rápida constituem importante proteção, limitando os danos causados pela dessecação em sementes maduras (BUCKERIDGE et al., 2000). Dentre os açúcares presentes nas sementes de café os mais comuns são as pentoses e as hexoses (glicose, frutose, galactose e manose), os quais estão ligados diretamente ao sabor adocicado do café, sendo com isso os mais importantes, pois devido à sua estrutura não sofrem hidrólise (SAATH, 2010). Com isso contribuem com a doçura da bebida do café, visto que, são considerados um dos atributos de sabor mais desejáveis nos cafés especiais, e participam de importantes reações (PEREIRA et al., 2002; CORADI et al., 2007; MARQUES et al., 2008). Segundo Mendonça et al. (2007), maiores concentrações de açúcares nos grãos crus de café contribuem expressivamente para as reações do processo de torração.
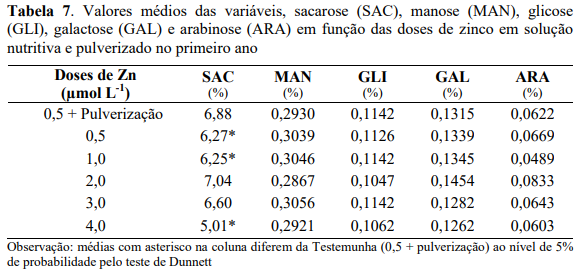
Observa-se na Tabela 7, que houve diferença significativa entre as doses de Zn fornecidas via solução nutritiva em comparação com a testemunha que recebeu, também, pulverizações foliares para os teores de sacarose (SAC), em que os teores de sacarose da testemunha foram superiores aos das doses de Zn (0,5; 1,0 e 4,0 µmol L-1) e não diferiram das demais doses. Para as demais variáveis não houve diferença significativa das doses de Zn em comparação à testemunha.
Os valores encontrados no presente trabalho não demostram nenhuma tendência de aumento dos demais açucares (manose, glicose, galactose e arabinose), com as pulverizações foliares com Zn, conforme melhora a qualidade da bebida com base na atividade da PPO e dos teores de sacarose.
Nos grãos de café, dentre os açúcares totais, os redutores (manose, glicose, galactose e arabinose) estão presentes em menores quantidades (SILVA et al., 2004; BORÉM et al., 2006; BORÉM et al., 2008c, 2008d; ABRAHÃO et al., 2009; SAATH, 2010) pois, predomina a sacarose, um açúcar não redutor. Segundo Lima, (2005), Knopp et al. (2006) e Mendonça et al. (2007) a concentração de sacarose nos grãos de café, pode variar de 1,9 a 10% na matéria seca. Maiores concentrações de açúcares nos grãos crus de café permitem um aumento na participação destes compostos nas reações do processo de torração (MENDONÇA et al., 2007), contribuindo com a doçura da bebida, que é considerado um dos atributos de sabor mais desejáveis nos cafés especiais (PEREIRA et al., 2002; CORADI et al., 2007; MARQUES et al., 2008). De acordo com Pereira et al. (2002); Coradi et al. (2007) e Marques et al.(2008), pode-se atribuir essa melhor qualidade às substâncias voláteis formadas a partir da combinação de tais açúcares com as proteínas no processo de torração.
Potássio lixiviado e condutividade elétrica
Em relação aos valores de potássio lixiviado (KL) e de condutividade elétrica (CE), verificou-se que houve efeito quadrático das doses de Zn (Figura 15), em que o potássio lixiviado nos grãos crus de café, apresentou na dose estimada de 2,11 µmol L-1 de Zn os menores valores (0,63 g kg-1) e teor foliar de 9,90 mg kg-1 ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ). Para a condutividade elétrica, verificou-se resultado semelhante ao do KL, apresentando na dose estimada de 2,05 µmol L-1 de Zn os menores valores de CE, correspondente a 193,9 µS cm-1 g -1, e teor foliar de 9,86 mg kg-1 ( Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ), enquanto que para a menor e maior dose de Zn, verificaram-se os maiores valores de CE, correspondente a 248,5 e 254,8 µS cm-1 g -1, respectivamente.
Os maiores valores de KL e CE foram verificados nas menores (0,2 µmol L-1) e nas maiores (4,0 µmol L-1) doses de Zn. Nas menores doses, isso possivelmente esteja relacionado à sua deficiência, pois sabe-se que em plantas deficientes em Zn ocorre o aumento da permeabilidade das membranas (CAKMAK e MARSCHNER, 1988; KAYA e HIGGS, 2001). Já para as doses estimadas de 2,11 µmol L-1 e 2,05 µmol L-1 respectivamente para KL e CE, referentes aos baixos valores de KL (0,63 g kg-1) e CE (193,9 µS cm-1 g -1) talvez estejam relacionados ao papel do Zn na manutenção da integridade das membranas dos grãos de café.
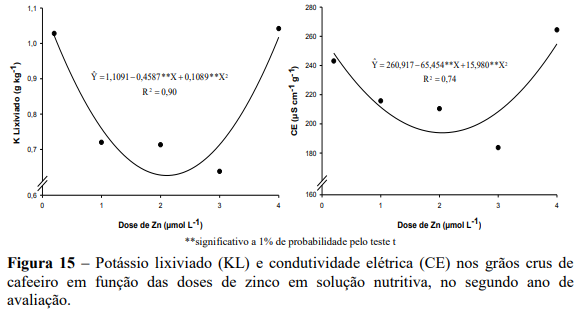
Segundo Poltronieri et al. (2011) o zinco, independentemente da forma de fornecimento, influencia positivamente a qualidade de grãos de café, caracterizada pelos baixos valores de condutividade elétrica e de potássio lixiviado dos grãos.
O aumento do KL e da CE nas maiores doses de Zn, pode estar relacionado a interações negativas do Zn com outros nutrientes, como também ao seu excesso provocando toxidez as plantas, com isso pode ter afetado a integridade da membrana e consequentemente provocado à lixiviação de K e o aumento da CE. Uma maior lixiviação de potássio, com o consequente aumento na condutividade elétrica, é um forte indicador de danos na membrana e na parede celular (GOULART et al. 2007).
A deterioração das estruturas de membranas reflete um processo de ruptura celular ocasionada pela rápida embebição de água pelos grãos e de acordo com Lima et al. (2008), quanto maior os danos em membranas, maior quantidade de eletrólitos é liberada na solução, resultando em maior valor de CE e LK. Segundo Illy et al. (1982) a desorganização celular permite que a água penetre e se difunda com maior facilidade com o aumento da intensidade dos danos celulares. Os testes de lixiviação de potássio e condutividade elétrica são utilizados em pesquisas como indicadores consistentes da integridade das membranas celulares. Os grãos com membranas mal estruturadas lixiviam mais solutos quando imersos em água (PRETE, 1992). Várias pesquisas demonstram que a piora da qualidade, se dá nos grãos em que a lixiviação de potássio e de condutividade elétrica aumentam (BORÉM et al., 2008; MARQUES et al., 2008; SANTOS; CHALFOUN; PIMENTA, 2009).
Percebe-se então que as doses de Zn influenciaram nas determinações de potássio lixiviado e de condutividade elétrica. Esse fato acentua a importância de uma boa nutrição das plantas de cafeeiro com o Zn, com a finalidade de se melhorar cada vez mais a qualidade do produto final que é o grão, o que resultará em melhores preços no mercado e maiores lucros para o produtor.
Nos dois anos de avaliação, os teores foliares de Zn observados nas folhas índice (ano1 Υ 5,4521 1,3667Zn; ˆ r 2 0,69 e ano2 Y 10,9162 1,5373Zn 0,4994Zn ; ˆ 2 R2 0,99 ) quando os atributos de qualidade estavam maximizados, variaram de 8 a 12,75 mg kg-1 (pontos de máximo ou mínimo) e coincidiram com a faixa considerada adequada por Martinez et al. 2003 na avaliação do estado nutricional do cafeeiro, que é de 8 a 12 mg kg-1.
Análise sensorial
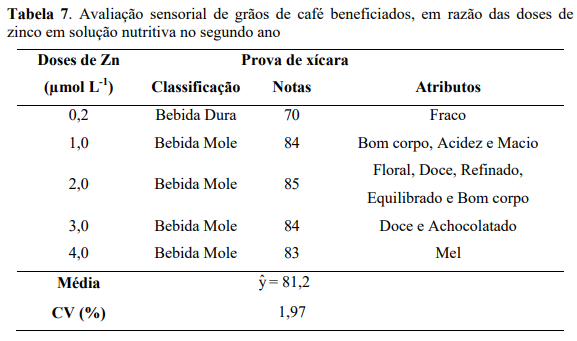
O café como bebida é normalmente classificado em sete grupos: estritamente mole, mole, apenas mole, dura, riada, rio e rio zona, em que as quatro primeiras consideradas bebidas finas e as três últimas bebidas fenicadas. Certos atributos podem ser adicionados a classificação, que podem levar à aquisição de características secundárias obtendo-se assim tipos de bebida tais como dura fraca, mole com bom corpo, doce e equilibrado entre outras (POLTRONIERI, 2010). No presente trabalho as características da bebida foram transformadas em escalas de valores permitindo uma avaliação quantitativa, como também foram incluídos, adicionalmente suas classificações e seus atributos (Tabela 8).
Pela avaliação sensorial (prova de xícara), verificou-se que não houve diferença significativa entre das doses de Zn, no entanto percebe-se que as maiores doses de Zn, proporcionaram atributos diferentes das menores doses, mas de modo geral correspondentes a bebidas mole, com exceção da menor dose de Zn que ficou como bebida dura (Tabela 8).
CONCLUSÕES
O incremento das doses de Zn até valores próximos a 2 µmol L-1 permitiu maximizar nos dois anos de avaliação, os atributos relacionados à qualidade da bebida, como a atividade da PPO, os teores de sacarose, trigonelina e a acidez titulável. Doses inferiores, ou superiores permitiram o incremento dos atributos relacionados com a perda de qualidade da bebida como, os fenóis totais, ácido 5-CQA, ácido málico, pH, potássio lixiviado e CE. Os teores foliares que se relacionaram aos pontos de máximo ou mínimo dos atributos de qualidade estudados variaram entre 8,0 e 12,75 mg kg-1 de Zn, ou seja estiveram dentro da faixa considerada adequada para o cafeeiro.
O fornecimento de Zn via foliar, suplementando o fornecimento via radicular, aumentou a produção de frutos, a atividade da PPO, os teores de sacarose, trigonelina e cafeína, atributos relacionados à qualidade da bebida do café, e, promoveu redução de fenóis totais, 5-CQA, índice de coloração, atributos relacionados à perda de qualidade da bebida.

CAPÍTULO 2
COMPOSIÇÃO QUÍMICA E QUALIDADE DE CAFÉ ARÁBICA SUBMETIDO A DOSES DE COBRE
O cobre embora exigido em pequenas quantidades pelo cafeeiro é essencial na constituição e na ativação de varias enzimas, atuando na oxidação de compostos fenólicos, formação de lignina e síntese de aminoácidos. Tais compostos estão diretamente relacionados à qualidade química dos grãos crus do café e por isso podem influenciar na qualidade da bebida. Objetivou-se com o presente trabalho avaliar a influência do Cu na composição química dos grãos e na qualidade de bebida do café. O experimento foi conduzido em casa de vegetação do Departamento de Fitotecnia (UFVMG), em sistema hidropônico com os tratamentos arranjados em delineamento inteiramente casualizado, com três repetições, sendo cada parcela constituída por 2 vasos, contendo uma planta de cafeeiro em cada vaso. Os tratamentos consistiram de doses crescentes de Cu (0,05; 0,1; 0,2; 0,4 e 0,8 µmol L-1) em solução nutritiva, mais um tratamento adicional que recebeu solução nutritiva contendo 0,05 µmol L-1 de Zn via solução, e 12 pulverizações foliares com sulfato de Cu a 0,2%. Foram colhidos os grãos maduros de cada tratamento, e após sua secagem e beneficiamento determinaramse: Acidez titulável (AT), fenóis totais, ácido 5-cafeoilquinico (5-CQA), a atividade da polifenoloxidase (PPO), os teores de sacarose, cafeína, trigonelina, K lixiviado, condutividade elétrica e analise sensorial. Verificaram-se no primeiro ano de avaliação respostas linear para a AT, atividade da enzima PPO e nos teores de sacarose para as doses de Cu. No segundo a AT, atividades da enzima PPO se ajustaram a função raiz quadrada e a sacarose ao modelo quadrático. Os teores de trigonelina no primeiro ano apresentaram resposta segundo a função raiz quadrada e para o segundo ano não se verificou efeito das doses de Cu. No primeiro ano os teores de fenóis totais e 5-CQA decresceram segundo ao modelo de raiz quadrada até um ponto de mínimo, com posterior incremento com as doses de Cu, para o segundo ano os fenóis totais se ajustaram ao modelo quadrático e o ácido 5-CQA a função raiz quadrada. As doses de Cu via solução nutritiva e pulverização foliar influenciaram positivamente a atividade da PPO, os teores de sacarose e trigonelina, e negativamente fenóis totais e 5-CQA, atributos relacionados à qualidade dos grãos de café. Os teores foliares que se relacionaram aos pontos de máximo ou mínimo dos atributos de qualidade estudados variaram entre 5,8 e 11,37 mg kg-1 de Cu.
INTRODUÇÃO
Devido às mudanças nas preferências do consumidor, a qualidade da bebida do café tem recebido atenção especial do setor cafeeiro, tornando-se a responsável pela difusão e adoção de novas tecnologias na cadeia produtiva do café (ABIC, 2013). Atualmente, o consumidor paga mais por produtos que possuam atributos associados à bebida, entre outros, aroma, sabor, acidez, corpo, adstringência e sabor residual (SAATH, 2010).
A qualidade da bebida é primordial para valorizar o produto (International Coffee Organization – ICO, 1991). Essa está associada aos diversos constituintes químicos do grão, responsáveis pelas características qualitativas da bebida (BYTOF et al., 2005; BYTOF et al., 2007; CHALFOUN; PARIZZI, 2008). E como o sabor característico do café como bebida é proveniente do grão, este é diretamente relacionado com as variedades e influenciado por tratos agrícolas (adubação no solo ou foliar), processos de secagem, fermentação, torrefação, moagem e envase (CAIXETA, 1999).
Independentemente da natureza dos cafés, a qualidade depende diretamente da sua composição química. Todos os atributos são consequência da presença de alguns componentes químicos, ou de combinações desses mesmos constituintes, em determinadas proporções (BUFFO; CARDELLI-FREIRE, 2004/2008; TOCI; FARAH, 2008). Assim, se torna possível definir a qualidade do café, relacionando-a quer com a quantificação de determinados constituintes, quer pela ausência de outros (CASAL et al. 2000; CASAL, 2004).
Vale ressaltar que a composição química dos grãos do café como também as suas variações qualitativas e quantitativas, já vem sendo analisadas por diversos pesquisadores, em função da espécie estudada, dos efeitos isolados do processamento, do ambiente de cultivo e do manejo (AVELINO et al., 2005; CAMPA et al., 2005; DUARTE et al., 2010; KNOPP et al., 2006; MONTEIRO; FARAH, 2012; RIBEIRO, 2013). Dentre os componentes físico-químicos do grão cru do café, se destacam os isômeros do ácido clorogênico (3-CQA, 4-CQA e 5-CQA), cafeína, trigonelina, fenóis e sacarose, os quais se mostram ter estreita relação com a qualidade sensorial da bebida e sua classificação (FARAH et al., 2006; FRANCA et al., 2005; SILVA et al., 2005).
Outra característica bioquímica do grão que apresenta maior correlação com a qualidade final do café é a atividade da enzima cúprica polifenoloxidase, pois de acordo com vários autores, se mostra diretamente relacionada com a qualidade da bebida do café (CARVALHO et al., 1994; MAZZAFERA et al., 2002; SILVA et al., 2009). Segundo Carvalho et al. (1994), cafés de melhor qualidade de bebida possuem elevada atividade enzimática da polifenoloxidase e elevado índice de coloração. Esses mesmos autores verificaram que as variações da atividade enzimática da polifenoloxidase, permitem separar as classes de bebida, mostrando para o café “riado e rio” atividades inferiores a 55,99 U g-1 de amostra; nos cafés de bebida “dura” atividades entre 55,99 e 62,99 U g-1 de amostra; nos cafés de bebida “mole” atividades entre 62,99 e 67,66 U g-1 de amostra e nos cafés de bebida “estritamente mole” atividades superiores a 67,66 U g1 de amostra, constatando assim um aumento significativo na atividade da polifenoloxidase à medida que o café se apresenta com melhor qualidade.
Dentre as condições de manejo, a adubação e a nutrição da planta com micronutrientes por via radicular ou foliar podem influenciar a composição química do grão verde, o qual, após torrado, produz compostos que conferem características de aroma e sabor ao café. Essa influencia da nutrição mineral foi verificada em vários trabalhos de pesquisa para nitrogênio e potássio (SILVA et al., 1999; SILVA et al., 2002; MALTA et al.,2003; CLEMENTE, 2010).
Em relação aos micronutrientes e sua influencia na formação de compostos nos grãos e na qualidade da bebida do café, poucos são os estudos, limitando-se ao efeito do zinco na qualidade da bebida do café (POLTRONIERI et al. 2011; MARTINEZ et al. 2013). Não há relatos sobre a relação entre o Cu via solução nutritiva e pulverização foliar com a qualidade dos grãos de café.
Mediante o exposto, e em virtude da busca pela produção de cafés de melhor qualidade percebe-se a necessidade de se pesquisar a relação da nutrição mineral com cobre e a qualidade da bebida do café. O cobre está diretamente envolvido na constituição e na ativação de varias enzimas. Uma dessas enzimas é a polifenoloxidase e oxidase de diamina, que catalisam a oxidação de compostos fenólicos a cetonas, precursores da lignina (MARSCHNER, 2012; MENGEL e KIRBY, 2001).
No contexto destas considerações, este estudo teve como objetivo avaliar a influência do cobre na produção, na composição química dos grãos de café e na qualidade de bebida.
MATERIAL E MÉTODOS
Sistema de cultivo e condução do experimento
O experimento foi conduzido em casa de vegetação do Departamento de Fitotecnia da Universidade Federal de Viçosa (UFV), situada no município de Viçosa, MG, localizada nas coordenadas 20º 45’S sul e 42º 51’O, com altitude média de 651 m, no período de agosto de 2010 a agosto de 2013. A temperatura média anual durante o período de condução do experimento foi de 22,4 ºC, com temperatura máxima de 45 ºC e mínima de 12ºC, dentro da casa de vegetação.
O delineamento experimental utilizado foi o inteiramente casualizado com três repetições, sendo cada parcela constituída por 2 vasos, contendo cada um, uma planta, totalizando 72 vasos.
Os tratamentos consistiram de doses de Cu em solução nutritiva. No primeiro ano de avaliação empregaram-se as doses de 0,05; 0,1; 0,2; 0,4 e 0,8 µmol L-1. No segundo ano de avaliação as doses foram ajustadas para 0,2; 0,4; 0,8; 1,6 e 3,2 µmol L-1 de Cu. A mudança nas doses de Cu se fez em virtude das plantas mostrarem deficiência aguda do nutriente, demostrando com isso que os valores utilizados na solução nutritiva eram insuficientes para produção de grão na segunda safra, com isso afetaria os resultados do experimento.
Nos dois anos houve um tratamento adicional em que se forneceu 0,05 µmol L-1 de Cu via solução nutritiva, complementando a dose com pulverizações foliares mensais à base de sulfato de Cu na concentração de 0,2%, sendo aplicado um total de 12 pulverizações a cada ano de cultivo. Os demais nutrientes foram fornecidos nas concentrações preconizadas por Clemente et al. (2013). Foram utilizadas mudas enxertadas em fenda cheia, de café da variedade Catuaí Vermelho IAC 99.
Foi utilizada a própria variedade IAC 99 como porta enxerto (cavalo) e enxerto (cavaleiro). Para o enxerto foram utilizados somente os ramos plagiotrópicos. O processo de enxertia foi feito com intuito de reduzir a fase vegetativa das plantas, favorecendo com isso uma frutificação precoce. Na fase pré-experimental as plantas foram conduzidas em recipientes retangulares de polietileno rígido (30 cm x 74 cm x 14 cm), com volume de 25 litros com solução nutritiva de 0,5 força e aeração forçada.
Posteriormente as mudas foram transplantadas para os vasos plásticos com capacidade de 11 L, contendo uma muda por vaso, preenchidos com areia lavada e uma camada de 2 cm de argila expandida no fundo recoberta por tela de sombrite de 50%, conforme Figura 1. No segundo ano de condução as plantas foram transferidas para vasos de 20 L de capacidade preparados da mesma forma descrita anteriormente. Os substratos (areia e argila expandida) utilizados, foram lavados com HCl a 18% e ácido oxálico a 1%, água e água desionizada conforme descrito por Martinez e Clemente (2011).
O sistema hidropônico utilizado foi o de três fases circulante. As plantas receberam diariamente aplicações de solução nutritiva no volume de 9,6 litros/vaso, cujo excesso foi drenado para um reservatório de descarga de 50 L. Esse reservatório foi equipado com eletrobomba que recalcava a solução drenada para os vasos, conforme a Figura 2. O controle da circulação da solução nutritiva foi realizado com o auxilio de um temporizador analógico programado para acionar a eletrobomba durante 1 minuto com vazão de 1,6 L/min por vaso e intervalos de 3 horas entre irrigações durante o dia. À noite o sistema permanecia desligado.
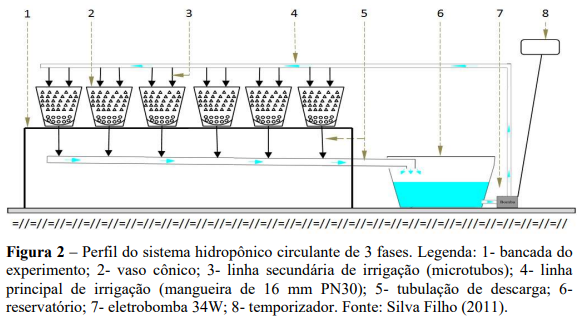
A solução nutritiva continha 6; 0,5; 3,23; 2,25; 1 e 1,75 mmol L-1 de N, P, K, Ca, Mg, S e 40; 12; 23; 0,5 e 0,3 µmol L-1 de Fe, Mn, B, Cu e Mo, respectivamente, conforme descrito por Clemente et al (2013). O volume da solução foi monitorado diariamente, e completado com água até o volume inicial de 50 L em cada reservatório. O pH da solução foi monitorado e mantido entre 5,5 e 6,0 mediante ajustes com a adição de HCl ou NaOH. Para determinar o momento da troca da solução nutritiva foram utilizados os valores de condutividade elétrica (CE), procedendo-se a troca ao verificar-se uma depleção correspondente a 30% da CE inicial. Foram utilizados os seguintes sais: KH2PO4, MgSO4, K2SO4, KNO3, Ca(NO3)2, NaNO3, CuSO4, ZnSO4, MnCl2, H3BO3, (NH4)6Mo7, FeCl2 e Na2EDTA.
A solução nutritiva foi contida em 12 reservatórios de plástico de 50 L, segundo os tratamentos e cada reservatório forneceu solução a seis vasos com uma planta cada. As soluções estoque de macronutrientes foram purificadas pelo método da APDC (amoniopirrolidinaditiocarbamato) e a solução de FeCl3 usando-se a resina trocadora especifica para Zn (Dowex 1X-8 de 50 mesh) conforme descrito por Martinez e Clemente (2011).
a) Avaliações
Produção
Os frutos foram colhidos individualmente no estádio de maturação cereja. Foram avaliadas as produções das duas plantas da parcela, sendo feita a contagem dos frutos de cada planta, sendo esse valor convertido em produção por planta (frutos/planta).
Posteriormente os frutos foram colocados para secar sobre leito de papel toalha, sobre bancadas, em casa de vegetação até atingirem 11 a 12% de umidade. Após a secagem, foram descascados obtendo-se assim os grãos beneficiados. Os grãos beneficiados foram pesados, obtendo-se o peso das duas plantas da parcela, sendo esse valor convertido em produção por planta (g/planta), e posteriores foram feitas as análises químicas.
b) Estado nutricional das plantas
O estado nutricional das plantas foi avaliado no início do pleno florescimento da cultura. Para realizar análise química foliar foram coletadas as folhas do terceiro ou quarto nó, contado do ápice para a base, dos ramos plagiotrópicos em floração. O material amostrado foi lavado em água desionizada e seco em estufa de ventilação forçada de ar a 70 ºC, por 72 horas. Em seguida o material foi moído em moinho tipo Wiley equipado com peneira de 20 mesh. Os teores de Zn foram determinados por espectrofotometria de absorção atômica conforme método adaptado de Malavolta et al. (1997).
c) Qualidade dos Grãos
Acidez Titulável
A acidez titulável foi determinada pelo método descrito pela AOAC (1990). Amostras de 1 g de café cru moído receberam 25 mL de água destilada e foram colocadas em agitador elétrico por 1 hora a 150 rpm, em seguida procedeu-se a filtragem em papel de filtro. Uma alíquota de 5 mL da solução filtrada foi adicionada a um erlenmeyer junto a 50 mL de água destilada e 3 gotas de fenolftaleína (1%), procedendo-se a titulação com NaOH (0,1 mol L-1). O resultado foi expresso em mL de NaOH 0,1 (mol/L)/100g de amostra.
Ácidos orgânicos
Os ácidos orgânicos (málico, tartárico e cítrico) foram determinados de acordo com Scherer et al., (2012). Uma amostra de 0,3 g, de grãos de café moído foi triturada em politron com 10 mL de água ultra-pura. Uma alíquota de 0,5 mL foi agitada com 1,5 mL da fase móvel que constiuiu-se de KH2PO4 0,01 mol L-1 (pH 2,6). O sobrenadante foi filtrado em filtro com membrana de 0,45 μm, e injetado diretamente em tubos de HPLC. As análises foram realizadas por cromatografia líquida de alta eficiência (CLAE), com coluna C18 de fase reversa.
Potencial hidrogeniônico (pH)
O pH foi determinado pelo método descrito pela AOAC (1990). Amostras de 2g de café cru moído receberam 50 mL de água destilada e foram colocadas em centrifuga por 1 hora a 150 rpm. Em seguida foi feita a filtragem em papel de filtro quantitativo de 9 cm de diâmetro e posteriormente foi feita a leitura com peagâmetro digital.
Fenóis Totais
A determinação dos compostos fenólicos totais na bebida do café foi realizada pelo método de Folin Denis, descrito pela Association of Official Agriculture ChemistsAOAC (1990). Uma amostra de 0,5 g de grãos foi extraída com 30 mL de metanol 50% sob agitação constante durante 15 minutos usando-se tubos com tampa rosqueada, seguido de filtragem em papel de filtro qualitativo no 4.
Em uma alíquota de 0,1 mL do extrato adicionaram-se 2,5 mL de uma solução aquosa do reativo de Folin-Ciocalteu (10%) e 2,0 mL de uma solução recém-preparada de carbonato de sódio a 7,5%. Manteve-se solução em um banho de água a uma temperatura de 50 ºC por 5 minutos. A absorbância foi registrada em um espectrofotômetro de UV/VIS a 760 nm. A curva de calibração foi feita com solução aquosa de ácido gálico nas concentrações de 10, 20, 30, 40 e 50 μg mL-1. As leituras foram feitas contra um branco. Os resultados foram expressos em equivalentes de ácido gálico.
Ácidos clorogênicos (3- cafeoilquinico, 4-cafeoilquinico e 5-cafeoilquinico)
Os ácidos clorogênicos foram extraídas com metanol aquoso (40 %) e clarificado com soluções de Carrez I e II (FARAH et al, 2005; TRUGO e MACRAE, 1984). As extrações foram realizadas da seguinte forma: amostras de café moído (0,5 g) foram extraídas com 80 mL de metanol 40% e transferidas para balões volumétricos de 100 mL. Em cada amostra foram adicionados 2 mL das soluções Carrez 1 e 2; após completar o volume para 100 mL e agitar, a mistura foi deixada em repouso por 10 minutos. O preciptado foi filtrado em papel de filtro Watman n0 1; posteriormente foi passado novamente em filtro com membrana de 0,45 μm, e injetado diretamente em tubos de HPLC. A curva de calibração foi plotada usando-se a mistura de isômeros em concentrações variando de 10 a 100 μg mL-1 .
Polifenoloxidase (PPO)
Uma amostra de 1 grama de café cru foi moído e colocada com 10 mL de tampão fosfato de sódio 0,1 mol L-1, pH 6b, a 40C, contendo 1% de ácido ascórbico. O material foi deixado em banho de gelo sob agitação por 10 minutos. Em seguida o extrato foi filtrado em papel de filtro comum, e o filtrado mantido em gelo para posterior dosagem da atividade.
O substrato utilizado para a dosagem da atividade da enzima foi o DOPA (3,4 – dihidroxifenilalanina), como usado por Carvalho et al. (1994) e Correa et al. (1997) – 8 mg de DOPA dissolvidos em 10 mL do tampão fosfato 0,1 mol L-1, pH 6,0.
A seguir, em uma alíquota de 900 μL do tampão fosfato 0,1 mol L-1, pH 6.0 contendo DOPA foram adicionados 100 μL do extrato. Imediatamente após a adição do extrato na cubeta de leitura foi feita a leitura de absorbância em 420 nm, e a partir daí a cada 15 segundos durante 5 minutos.
Índice de coloração
O índice de coloração foi determinado pelo método descrito por Singleton (1966), adaptado para café. Uma amostra de 1 g de café cru moído foi colocado em erlenmeyer ao qual foram adicionados 25 mL de água destilada. A amostra foi homogeneizada em agitador por 1 hora. Procedeu-se a filtragem em papel de filtro quantitativo de 9 cm de diâmetro, sendo tomada uma alíquota de 5 mL do filtrado aos quais foram adicionados a 10 mL de água destilada. As amostras foram deixadas em repouso por 20 minutos e lidas em espectrofotômetro ajustado para 425 nm.
Cafeína e trigonelina
Os componentes químicos cafeína e trigonelina foram determinados pelo método descrito por Mazzafera (1994) e Vitorino et al. (2001). Os grãos de café foram moídos em moinho de bolas e uma amostra de 0,1 g foi extraída com 10 mL de metanol 80% durante 1 hora em banho-maria (80 0C), com ocasional agitação. Depois de resfriarem em temperatura ambiente, uma alíquota de 2 mL foi centrifugada em durante 10 minutos. O sobrenadante foi filtrado em filtro com membrana de 0,45 μm, e injetado diretamente em tubos de HPLC. As análises foram realizadas por cromatografia líquida de alta eficiência (CLAE), com coluna Acclaim 120 C18 de fase reversa. O sistema encontrava‑se acoplado a um fotodetector de arranjo de diodos que por sua vez estava conectado por interface a um microcomputador para processamento de dados.
A análise de cafeína foram feitas tendo como solvente o metanol e água na proporção de 40:60 e fluxo de 1 mL minuto-1, sendo detectada em 272 nm. A quantificação foi feita por comparação com o padrão de cafeína pura.
As análises de trigonelina foram feitas tendo metanol, água e ácido acético na proporção de 20:79:1 e fluxo de 1 mL minuto-1, sendo detectada em 265 nm. A quantificação foi feita por comparação ao padrão externo de trigonelina pura. A curva de calibração para cafeína e trigonelina foi feita em concentrações variando de 0 a 175 μg mL-1 .
Proantocianidinas
Uma amostra de 0,3 g de café moído foi extraído com 10 mL de metanol 80% sob agitação constante durante 24 horas em temperatura ambiente, usando-se tubos com tampa rosqueada, seguido de filtragem em papel de filtro qualitativo no 4.
Transferiu-se 0,10 mL do extrato bruto para um tubo de ensaio e adicionaram-se 2,0 ml de uma solução recém preparada de vanilina em ácido sulfúrico 70% na concentração de 1g/100mL. A solução resultante foi colocada em banho de água a 50 ºC por 15 minutos. Mediu-se a absorbância a 500 nm. Juntamente com os extratos preparou-se uma curva de calibração com catequina nas concentrações de 2, 5, 10, 20 e 30 μg mL-1. Tanto as amostras quanto os padrões da curva de calibração passaram pelo mesmo tratamento. A leitura foi feita contra um branco e os resultados expressos em equivalentes de catequina (HAGERMAN, 2002 e HASLAM, 1989).
Sacarose
Uma amostra de 0,05 g foi colocada em tubo de centrífuga, na qual foi adicionado 1 mL de etanol 80%, em seguida foram imersos em banho de água (80 0C) durante 20 minutos. Posteriormente as amostras foram centrifugadas e o sobrenadante vertido em outro tubo de centrífuga. Sobre o resíduo foi adicionado 1 mL de etanol 80% e o processo foi repetido novamente. Os sobrenadantes foram centrifugados durante 1 minuto, passado em filtro de membrana de 0,45μm e injetado em tubos de HPLC.
Para determinação da sacarose foi utilizado um detector de índice de refração e uma coluna SP 0810 (300mm X 8 mm) em temperatura de 80 0C; utilizou-se água ultrapura como fase móvel em fluxo de 1 mL/minuto. A curva de calibração foi feita nas concentrações de 0; 0,5; 1,0 e 1,5 mg mL-1 utilizando-se sacarose pura (SLUITER et al. 2008).
Glicose, manose, arabinose e galactose
Os açucares redutores (glicose, manose, arabinose e galactose) foram determinados pelo método descrito por SLUITER et al., (2008). Amostras de café (0,5 g) foram submetidas à hidrólise ácida com 3 mL de ácido sulfúrico 72% e mantidas em banho-maria (50 0C) durante 7 minutos. Posteriormente ao pré-tratamento foram adicionados 84 mL de água ultra-pura, as amostras foram autoclavadas durante 45 minutos (121 0C). Depois de resfriadas a temperatura ambiente, uma alíquota de 10 ml foi transferida para enlenmeyer e o pH corrigido para valores entre 4 e 6 com carbonato de cálcio puro. O sobrenadante foi coletado e passado em membrana de filtro de 0,45 μm e injetados em tubos para HPLC.
Para determinação desses açúcares foi utilizado um detector de índice de refração a 50 0C e uma coluna SP 0810 (300mm X 8 mm) em temperatura 80 0C; utilizou-se água ultra-pura como fase móvel e fluxo de 0,6 mL minuto-1. A quantificação foi feita por comparação com os padrões de glicose, manose, arabinose e galactose. A curva de calibração foi construída nas concentrações de 0,1; 0,5; 1,0; 1,5; 2,0 e 2,5 mg ml-1 para todos os açúcares.
Potássio lixiviado e condutividade elétrica
O potássio lixiviado e condutividade elétrica foram determinados pelo método descrito por Prete (1992). Amostras de 50 grãos de café beneficiado foram colocadas em copos plásticos de 180 mL, aos quais foram adicionados 75 mL de água destilada; em seguida foram colocadas em estufa ventilada por 5 horas. Após esse tempo foram realizadas leituras das condutividades eletricas. De cada amostra retirou-se uma alíquota para realizar a leitura do K lixiviado em fotômetro de chama.
Teor de água
O teor de água foi determinado pelo método padrão da estufa a 105±1ºC por 24 horas, de acordo com metodologia proposta por Mara (1992).
Análise sensorial
A prova de xícara foi realizada no segundo ano de produção, por provadores profissionais da “3 Irmãos Corretora de Café”. Para realização das análises estatísticas os resultados obtidos para classificação da bebida pela prova de xícara foram convertidos em valores numéricos. Estes valores constam na tabela 1.

d) Análise estatística
Os dados obtidos foram submetidos à análise de variância (ANOVA) e regressão. Aplicou-se análise de regressão para avaliar os efeitos de doses de Zn e teste de Dunnett para comparar as doses de Zn com o tratamento testemunha. Os modelos foram selecionados com base na significância, dos coeficientes de regressão utilizando-se o teste “t”, adotando-se o nível de 5% de probabilidade, no fenômeno biológico e no coeficiente de determinação. Os dados foram analisados usando-se o programa SAEG 9.0 (Sistema de Análise Estatística e Genética) (SAEG, 2007).
RESULTADOS E DISCUSSÃO
a) Produção
Nos dois anos houve efeito significativo das doses de Cu para produção de grãos de cafeeiro. No primeiro ano o aumento da dose de cobre na solução nutritiva proporcionou efeito linear crescente para produção de grãos de cafeeiro, sendo os teores foliares de 5,80 mg kg-1 de Cu ( Υ 2,8444 3,7018Cu ˆ ; r 0,88 2 ), os que se relacionaram ao ponto de maior produção (21 g por planta) (Figuras 3A). No segundo ano a produção de grãos se ajustou ao modelo quadrático, apresentando o ponto de máxima produção (38,6 g por planta) na dose estimada de 1,45 µmol L-1 de Cu e teor foliar de 7,20 mg kg-1 de Cu ( Υ 3,1025 3,1907Cu ˆ ; r 0,98 2 ) (Figura 3B).
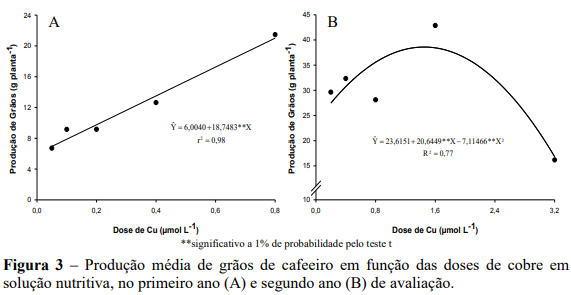
Segundo Pilon et al. (2006) e Marschner (2012) o cobre desempenha papel na fotossíntese, respiração, distribuição de hidratos de carbono, metabolismo de proteínas, atividade antioxidante, lignificação e formação dos grãos de pólen.
Sancenón et al. (2004), ao estudarem plantas de Arabidopsis transgênicas com baixa expressão ao transportador de Cu, demostraram que a formação anormal do grão de pólen pode ser consideravelmente reduzida com a adição de cobre as plantas. Graham (1975), citado por Marschner (2012) afirmou que as principais causas da redução na produção de grãos e frutos, em plantas deficientes em cobre é a inibição da formação das anteras, ao menor número de grãos de pólen por anteras, e a perda da viabilidade do pólen.
A redução na produção de frutos em doses superiores a 1,45 µmol L-1 de Cu no segundo ano de avaliação pode estar relacionada à interação negativa com outros cátions, em que o excesso de cobre pode ter induzido deficiência de Fe, Zn e Mn em razão da semelhança dos raios iônicos (BOARDMAN e MCGUIRE, 1990; SAGARDOY et al, 2009).
Na Tabela 3, são apresentados os valores médios de número de frutos por plantas (NF), produção de grãos beneficiados, massa de 100 grãos (MAS100G) e dos frutos de café em coco, obtidos para as diferentes doses de Cu e para o tratamento que recebeu pulverizações foliares mensais com Cu (Testemunha). Apenas as doses de Cu 0,05; 0,1 e 0,8 µmol L-1 diferiram de sua testemunha (pulverização foliar com Cu) com relação ao número de frutos por plantas (FP). O número de frutos produzido pela testemunha foi superior que o das menores doses de Cu (0,05 e 0,1 µmol L-1), e inferior ao da dose 0,8 µmol L-1 de Cu. A produção de grãos, massa de 100 grãos (PES100G) e dos frutos, nas doses de Cu de 0,05; 0,1; 0,2 e 0,4 µmol L-1 foram inferiores aos da testemunha, enquanto que na maior dose de Cu (0,8 µmol L-1) não diferiram dela.
Verifica-se, neste trabalho que o fornecimento de Cu via foliar destacou-se quando as doses fornecidas via solução nutritiva eram baixas, demonstrando com isso, que o fornecimento do Cu via foliar, é uma forma alternativa de suprir as necessidades das plantas de café, quando o fornecimento via radicular for insuficiente.
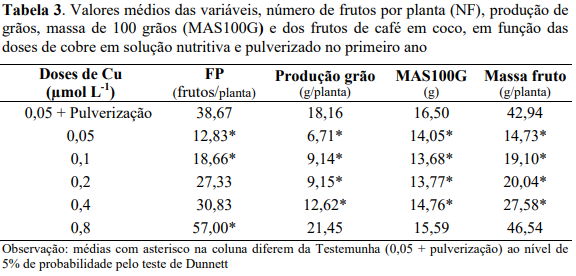
b) Qualidade dos Grãos
Acidez titulável
Nos dois anos houve efeito significativo das doses de Cu para a acidez titulável. No primeiro ano a acidez titulável apresentou incremento linear para as doses de cobre, com o maior valor de acidez titulável (52,12 mL NaOH 100g-1) verificado na dose máxima aplicada de Cu e teor foliar de 5,8 mg kg-1 de Cu ( Υ 2,8444 3,7018Cu ˆ ; r 0,88 2 ) (Figura 4A). No segundo ano a acidez titulável se ajustou ao modelo raiz quadrática, apresentando o menor valor (115,57 mL NaOH 100g-1) na dose estimada de 1,75 µmol L-1 de Cu e teor foliar de 9,75 mg kg-1. (Υ 3,1025 3,1907Cu ˆ ; r 0,98 2 ) (Figura 4B).
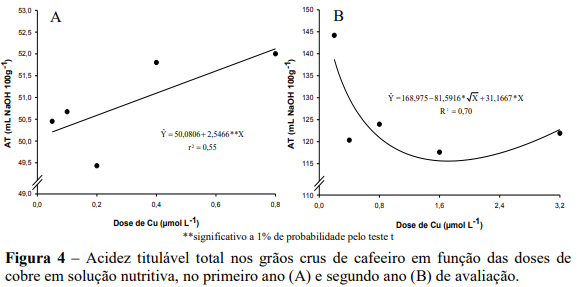
Observou-se no primeiro ano uma relação direta da AT com a produção de grãos (Figura 3A), com o maior valor de AT (52,12 mL NaOH 100g-1), na maior dose de Cu (0,5 µmol L-1) proporcionado a maior produções de grãos (21 g por planta). No segundo ano observou-se uma baixa concordância da produção de grãos (Figura 3B) com os valores de AT, verificando-se na dose de Cu em que a acidez foi mínima (1,75 µmol L-1 na AT) uma pequena redução na produção de grãos (37,95 g por planta). Comparando os valores estimados de acidez titulável total (Figura 4A e 4B), com os encontrados por Carvalho et al. (1994), observa-se que, apesar de ter ocorrido diferença significativa nas doses de Cu, o menor e o maior valor da acidez titulável encontrado no primeiro ano (50,21 e 52,12 mL NaOH 0,1N 100g-1) e no segundo ano (115,57 e 138,45 NaOH 0,1N 100g-1), estão abaixo da faixa de classificação como café de bebida dura, riada e rio (250,4; 272,2 e 284,5 mL de NaOH 0,1N 100g-1), ou seja, apesar de ter ocorrido diferença significativa na acidez em decorrência das doses Cu essa diferença não tem grande impacto na qualidade dos grãos de café. No presente trabalho a qualidade do café se enquadra em cafés especiais, pelos baixo valores de acidez.
De acordo com Carvalho et al. (1994) a acidez titulável (AT) dos grãos de café tem uma relação inversa com a qualidade da bebida do café, pois cafés de melhor qualidade possuem maior atividade enzimática da polifenoloxidase e índice de coloração e, menor acidez titulável. Os mesmos autores ressaltam a importância da utilização da acidez total titulável em conjunto com a atividade da polifenoloxidase e o índice de coloração como suporte, a fim de melhorar a classificação sensorial da bebida do café.
Ácidos orgânicos
No primeiro ano de avaliação não se verificou efeito significativo da dose de Cu para os teores dos ácidos cítrico, tartárico e málico nos grãos de café. Os resultados apresentados no segundo ano (Figuras 5A, 5B e 5C) demonstram que as doses de Cu influenciaram significativamente os teores dos ácidos tartárico, málico e cítrico. Pode-se observar nos dados apresentados (Figura 5A), que o ácido tartárico se ajustou ao modelo raiz quadrática com o maior teor (2,72%) verificado na dose estimada de 1,0 µmol L-1 de Cu e teor foliar de 6,29 mg kg-1 de Cu ( Υ 3,1025 3,1907Cu ˆ ; r 0,98 2 ), no entanto para a maior dose de Cu (3,2 µmol L-1) o teor do ácido reduziu-se 25%, apresentando-se com 2,04% em comparação ao valor da dose estimada (2,72%).
O ácido cítrico se ajustou ao modelo quadrático, com o maior teor (1,16%) encontrado na dose estimada de 0,63 µmol L-1 de Cu, e teor foliar de 5,11 mg kg-1 de Cu (Υ 3,1025 3,1907Cu ˆ ; r 0,98 2 ). Com o incremento das doses de Cu acima desse valor houve redução nos teores desse acido que atingiu na maior dose de Cu (3,2 µmol L -1) o menor teor (1,05%). Isso corresponde a uma redução de 10% em comparação a dose estimada no ponto de máximo (1,16%) (Figura 5B).
Em relação ácido málico os resultados foram semelhantes aos dos demais ácidos, com o maior teor (0,30%) apresentado na dose estimada de 1,97 µmol L-1 de Cu e teor foliar de 9,39 mg kg-1 de Cu (Υ 3,1025 3,1907Cu ˆ ; r 0,98 2 ) (Figura 5C).
Segundo Feldman et al. (1969), a acidez dos grãos de café é constituída predominantemente por ácidos não voláteis, tais como oxálico, málico, cítrico, tartárico, pirúvico. Esses ácidos são originários de diversas rotas bioquímicas, bem como da fermentação por microorganismos dos açúcares existentes na polpa e na mucilagem dos frutos (CHALFOUN, 1996).
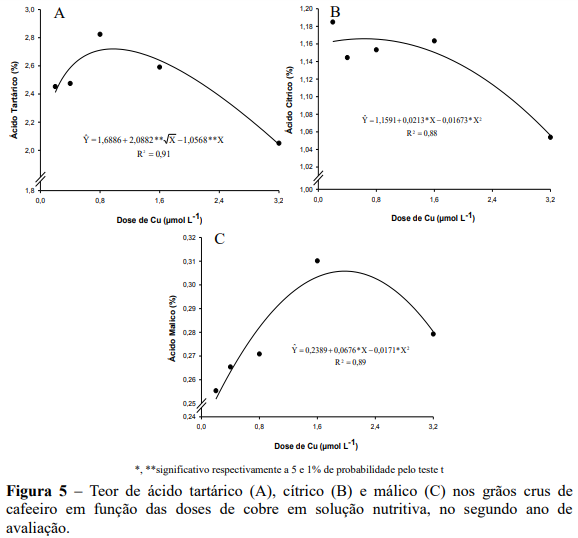
Na tabela 2, são apresentados as comparações entre os valores de acidez titulável, os teores dos ácidos cítricos, tartárico, málico e pH obtidos com as diferentes doses de Cu e o tratamento adicional (testemunha), que recebeu pulverizações foliares com o elemento. Verifica-se que não houve diferença significativa da acidez titulável entre a testemunha e os demais tratamentos., Para as outras variáveis como ácido cítrico, ácido tartárico e ácido málico, os teores dos ácidos cítrico e tartáricos da testemunha foram inferiores aos das doses de Cu (0,1 e 0,4 µmol L-1) e (0,1; 0,2 e 0,4 µmol L-1) respectivamente. Para o ácido málico verificou-se o inverso, o teor do ácido na testemunha foi superior ao da dose de Cu 0,05 µmol L-1 e não diferiu do das demais doses.
Para os valores de pH (Tabela 3) houve diferença significativa da testemunha em relação a todas as doses de Cu, em que os valores do pH da testemunha foram inferiores aos valores das doses de Cu (0,05; 0,1; 0,2; 0,4 e 0,8 µmol L-1).
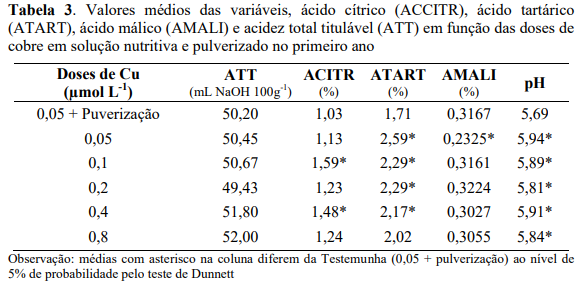
O pH é um parâmetro de muita importância na aceitação do produto pelo consumidor. Para café beneficiado grão cru os valores de pH encontram-se na faixa de 5,30 a 5,90 (OIC, 1992; BARRIOS, 2001; SIQUEIRA; ABREU, 2006). No presente trabalho obtiveram-se valores na faixa de 5,69 a 5,94%, tendo a testemunha apresentado o menor valor de pH (Tabela 3).
Potencial hidrogeniônico (pH)
Não houve variação nos valores de pH com as doses de Cu da solução nutritiva no primeiro ano de avaliação. No segundo ano observou-se efeito quadrático nas doses de Cu sobre o pH, verificando-se o menor valor (6,05) na dose estimada de 1,55 µmol L-1 de Cu e teor foliar de 8,05 mg kg-1 de Cu ( Υ 3,1025 3,1907Cu ˆ ; r 0,98 2 ) (Figura 6). Para a maior e menor dose de Cu verificaram-se os maiores valor ES de pH correspondendo a 6,11 a 6,14 respectivamente. Pinto et al. (2002) obtiveram em grãos de café torrado, as bebidas estritamente mole, mole e riada para os menores valores de pH (5,30 a 5,32).
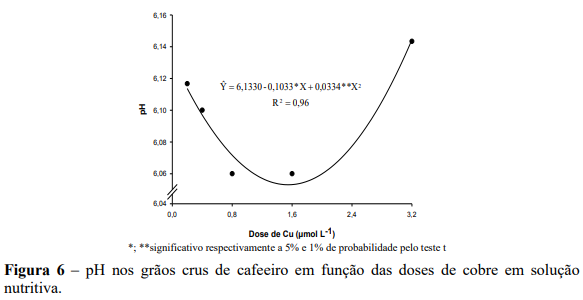
Em relação ao teor de fenóis totais, verificou-se efeito significativo nos dois anos para as doses de Cu. No primeiro ano, em resposta às doses de Cu, os teores de fenóis totais decresceram e se ajustaram ao modelo de raiz quadrada, com o ponto de mínima (5,3%) verificado na dose estimada de 0,6 µmol L-1 de Cu e teor foliar de 4,7 mg kg-1 de Cu ( Υ 2,8444 3,7018Cu ˆ ; r 0,88 2 ) (Figura 7A).
Fenóis Totais
No segundo ano houve declínio nos teores de fenóis que se ajustaram ao modelo quadrático, com o menor teor (6,10 %) verificado na dose estimada de 1,55 µmol L-1 e teor foliar de 8,05 mg kg-1 de Cu (Υ 3,1025 3,1907Cu ˆ ; r 0,98 2 ) (Figura 7B).
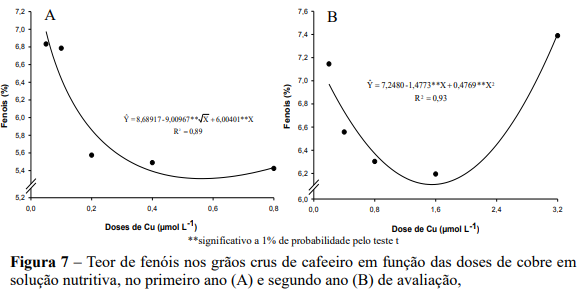
A redução nos teores de fenóis com as maiores doses de Cu está diretamente relacionada ao papel do Cu no metabolismo secundário das plantas, ou seja, no processo de lignificação e formação de substâncias melanóticas, pois as enzimas que oxidam os fenóis em lignina e outros compostos, como lacase e as peroxidases são ativadas pelo Cu. Consequentemente quanto maior o teor de cobre na planta maior será atividade dessas enzimas, contribuindo com isso para redução dos teores de fenóis. Enquanto que a deficiência de Cu diminui a atividade dessas enzimas, levando ao acúmulo de fenóis e à diminuição da lignificação (ROBSON et al., 1981).
Ácidos clorogênicos (3- cafeoilquinico, 4-cafeoilquinico e 5-cafeoilquinico)
Nos dois anos de avaliações os teores do ácido 5-cafeoilquínico (5-CQA) se ajustaram a função raiz quadrada nas doses de Cu. Verificou-se no primeiro ano que os teores de 5-cafeoilquínico decresceram com posterior estabilização com aumento das doses de Cu, com o menor teor (0,87 % de 5-CQA) verificado na dose estimada de 0,5 µmol L-1 de Cu e teor foliar de 4,7 mg kg-1 de Cu (Υ 2,8444 3,7018* Cu ˆ ; r 0,88 2 ) (Figura 8A). Efeito semelhante foi observado para o segundo ano de avaliação, em que os teores de 5-cafeoilquínico decresceram com posterior aumento com o incremento das doses de Cu, com o menor teor (0,97%) verificado na dose estimada de 1,62 µmol L-1 de Cu e teor foliar de 8,27 mg kg-1 de Cu ( Υ 3,1025 3,1907**Cu ˆ ; r 0,98 2 ) (Figura 8B).
Essa redução nos teores do 5-CQA com o aumento das doses de Cu, esta inversamente proporcional à atividade da PPO (Figura 9), em que à medida que os teores do 5-CQA decrescem ou aumentam, o inverso ocorre com a PPO. De acordo com Carvalho et al.(1989), existem indícios da ocorrência de maior concentração de polifenóis, como o caso do ácidos clorogênicos (CGA), em cafés de pior qualidade. Farah (2004) encontrou os maiores teores de 5-CQA em cafés com qualidade de bebida inferior.
No primeiro ano não se verificou efeito das doses de Cu para os ácidos 4- cafeoilquínico (4-CQA) e 3-cafeoilquínico (3-CQA). No segundo ano houve efeito significativo dos teores do ácido 4-CQA e 3-CQA nas doses de cobre. Os teores do ácido 4-CQA diminuíram com o incremento das doses de Cu depois estabilizaram-se, se ajustando ao modelo quadrático, com o menor teor (0,71%) verificado na dose estimada de 2,59 µmol L-1 de Cu e teor foliar de Cu de 11,37 mg kg-1 (Υ 3,1025 3,1907Cu ˆ ; r 0,98 2 ) (Figura 8C). Os teores do ácido 3-CQA aumentaram com o incremento das doses de Cu, com os valores se ajustando ao modelo quadrático, com o maior teor (1,06%) verificado na dose estimada de 1,86 µmol L-1 de Cu e teor foliar de Cu de 9,03 mg kg-1 ( Υ 3,1025 3,1907Cu ˆ ; r 0,98 2 )(Figura 8D). Esse resultado corresponde ao incremento de 15% no teor do ácido 3-CQA, em relação a menor dose de cobre, que proporcionou teor de 0,92% do isômero. Para a dose máxima de Cu houve redução no teor do ácido 3-CQA de 9% em comparação ao valor da dose estimada no ponto de máximo (1,06%).
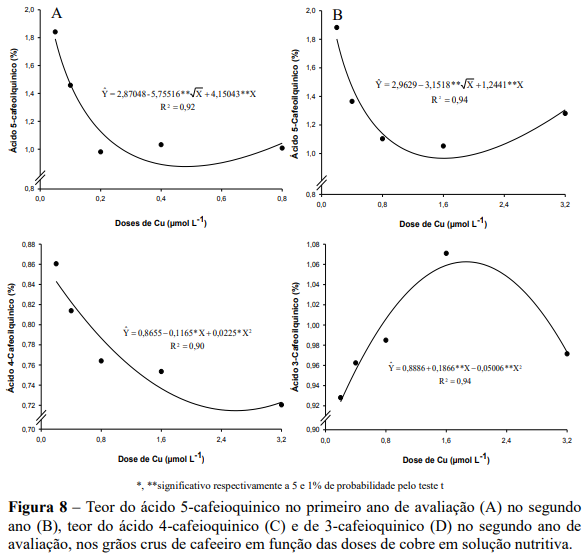
Esse aumento nos teores do ácido 3-cafeoilquínico com o aumento das doses de Cu, esta diretamente proporcional à atividade da PPO (Figura 9), em que à medida que os teores do 3-CQA aumentam ou diminuem, o mesmo ocorre para a PPO. Essa variação é inversa a que ocorre para os teores de fenóis totais (Figura 7), 5-CQA e 4- CQA cujas concentrações decresceram com o aumento da dose de Cu.
De acordo com Salva e Lima (2007), cafés que contêm menos ácidos clorogênicos proporcionam bebidas menos adstringentes e com sabor mais característico de café. Esse mesmos autores relatam que o amargor, a adstringência e o gosto de mofo da bebida se devem a concentração de ácidos clorogênicos e das proporções em que os diferentes CGAs são encontrados nos cafés crus. Dentre os grupos que compõe os CGAs do café, 5-CQA é o mais abundante em sementes de café.
Segundo Farah (2009) os ácidos clorogênicos oferecem proteção em relação a estresses abióticos, tais como aqueles associados à temperatura alta, estresse hídrico e biótico, exposição à luz UV e deficiência de nutrientes. Além disso, os ácidos clorogênicos contribuem para o processo de fermentação e influencia marcantemente a qualidade de xícara do café (FARAH et al., 2006).
Os compostos fenólicos possuem alto potencial redox, sendo assim, substratos preferenciais no combate ao estresse. Além da funcionalidade, contribuem expressivamente como precursores de flavor no café torrado (ARRUDA et al. 2012; LIMA et al. 2010). No processo de torrefação os ACGs são precursores dos ácidos fenólicos livres e, por conseguinte, dos compostos fenólicos voláteis que participam da formação do aroma do café (MOREIRA et al. 2000). Os ácidos clorogênicos reagem durante a torra, produzindo compostos ácidos, lactonas e outros derivados fenólicos responsáveis pelo aroma e sabor do café, acidez final e adstringência da bebida (LÓPEZ-GALILEA et al. 2007).
Polifenoloxidase (PPO)
No primeiro ano a atividade da polifenoloxidase (PPO) aumentou linearmente com a dose de cobre, em que a maior atividade da enzima (80,76 U. g-1 de amostra) foi verificada na dose máxima aplicada (0,8 µmol L-1 de Cu) (Figura 9A). Nessa condição as plantas apresentavam teor foliar de 5,8 mg kg-1 de Cu (Υ 2,8444 3,7018Cu ˆ ; r 0,88 2 ). Esse resultado corresponde ao incremento de 23% no aumento da atividade da PPO, em relação à menor dose de cobre, que permitiu obter atividade da enzima de 65,53 76 U. g-1 de amostra.
No segundo ano a atividade da polifenoloxidase (PPO) respondeu às doses de Cu segundo ao modelo de raiz quadrada, verificando-se a maior atividade da enzima (81,35 U. g-1 de amostra) na dose estimada de 0,78 µmol L-1 de Cu (Figura 9B), correspondente a concentração foliar de 5,6 mg kg-1 de Cu ( Υ 3,1025 3,1907Cu ˆ ; r 0,98 2 ). Enquanto para a menor e maior dose de Cu obtiveram-se as menores atividades da PPO, que corresponderam 77,85 e 65,23 U. g-1 de amostra respectivamente.
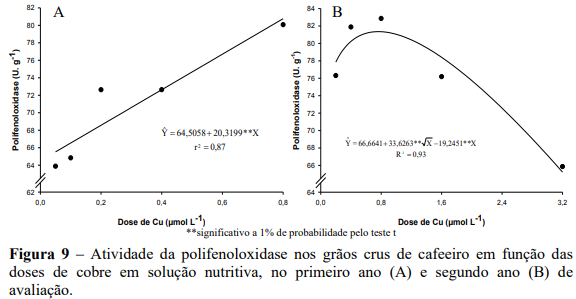
Observou-se no primeiro ano uma relação direta da atividade da PPO com a produção de grãos (Figura 3A), com a maior atividade da PPO (80,76 U. g-1 de amostra), na maior dose de Cu (0,5 µmol L-1) proporcionando a maior produção de grãos (21 g por planta). No segundo ano observou-se uma baixa concordância da produção de grãos (Figura 3B) com atividade da PPO, verificando-se na dose estimada de Cu (0,78 µmol L-1 maior atividade da PPO), uma baixa produção de grãos (35,58 g por planta).
Na classificação proposta por Carvalho et al. (1994) com base na atividade da PPO, no primeiro ano de avaliação, pode-se atribuir aos grãos de café na dose máxima de Cu a classificação na faixa de bebida “estritamente mole”, enquanto que para a menor dose de Cu os grãos de café seriam classificados como bebida “mole”. Para o segundo ano, seria atribuído aos grãos de café na dose de Cu estimada como ponto de máximo e na menor dose a classificação “estritamente mole” e para a maior dose de Cu os grãos de café seriam classificados como bebida “mole”.
Esses resultados demonstram que as baixas concentrações de Cu (primeiro ano) como também as altas (segundo ano), podem ter efeito negativos na atividade da enzima PPO, isso consequentemente poderá refletir na baixa qualidade do grão e da bebida do café. O aumento na atividade da PPO devido à aplicação do Cu, se deve ao fato desse nutriente participar da estrutura da enzima como grupo prostético, o que favoreceu a formação de maior quantidade de enzimas nos grãos, e consequentemente, proporcionou maior atividade. A polifenoloxidase é uma enzima cúprica que, de acordo com vários autores, se mostra diretamente relacionada com a qualidade da bebida do café (CARVALHO et al., 1994; CHAGAS et al., 1996; MAZZAFERA et al., 2002; SILVA et al., 2009).
Os valores da atividade da PPO obtidos nas maiores doses de Cu são bastante superiores aos preconizados por Carvalho et al. (1994), demonstrando que o Cu influencia a atividade da PPO e, como consequência na qualidade da bebida do café.
Índice de coloração
Nos dois anos de avalição não se verificou efeito das doses de Cu para o índice de coloração (Tabela 5). Os grãos de café com maior atividade da polifenoloxidase, apresentaram tendência de maior IC conforme Carvalho et al. (1994), apesar de não existirem diferenças significativas para o IC entre as doses de cobre (Tabela 5). Cafés de melhor qualidade possuem maior atividade da PPO e IC, conforme pesquisas desenvolvidas por, Carvalho et al. (1994), Leite e Carvalho (1994), Chagas et al. (1996), Silva et al. (2002) e Silva et al. (2009). Carvalho et al. (1994) estabeleceram que cafés com índices de coloração iguais ou superiores a 0,65 se enquadram nas classes de cafés "duro", "apenas mole", "mole" e "estritamente mole". Os índices de coloração inferiores a 0,65 (D.O. 435 nm) são classificados como "rio" e "riado", ou seja, cafés não exportáveis.
Na presente pesquisa em que a bebida foi classificada como "mole" (Tabela 11) independentemente da dose de Cu, os valores de IC variaram entre 0,74 (segundo ano) e 1,22 (D.O. 435 nm) (primeiro ano). Esses resultados não corroboram com os de Corrêa et al. (1997) em que o índice de coloração possibilitou a distinção entre as bebidas dura, apenas mole, mole e estritamente mole. Porém os valores do índice de coloração encontrados por esses autores foram: 0,47, 0,54, 0,63, e 0,72 respectivamente.
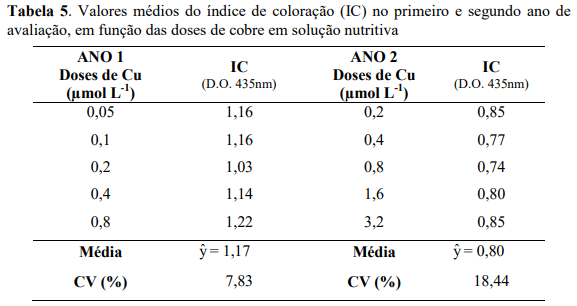
Com base nos resultados obtidos (Tabela 6), observa-se que houve diferença significativa da testemunha pulverizada para os teores de fenóis totais, os isômeros do acido clorogênico (3CQA e 5CQA), da enzima PPO e do índice de coloração em comparação as doses de Cu fornecidas exclusivamente na solução nutritiva.
Pela análise dos compostos fenólicos totais e do ácido 5-CQA, observou-se diferença significativa da testemunha em comparação as menores doses de Cu (0,05 e 0,1 µmol L-1), em que as menores doses de Cu apresentaram valores superiores de fenóis totais e do ácido 5-CQA. Esses maiores teores de fenóis totais e do ácido 5-CQA nas menores doses de Cu está diretamente relacionada ao papel do Cu no metabolismo secundário das plantas, ou seja, no processo de lignificação e formação de substâncias melanóticas, pois o baixo suprimento de Cu nas menores doses, faz com que a atividade das enzimas que oxidam os fenóis em lignina e outros compostos, como lacase e as peroxidases sejam reduzidas, pois dependem do Cu para ativá-las.
Existem indicações que há maior concentração de compostos fenólicos totais em cafés de pior qualidade. Pinto et al. (2002), em grãos de café arábica, classificados em diferentes padrões de bebidas, determinaram maior teor de compostos fenólicos nos cafés de bebida rio, quando comparados aos classificados como bebida mole.
O teor do isômero do ácido clorogênico (3-CQA) na testemunha diferiu das doses de Cu (0,05 e 0,4 µmol L-1), em que o teor do 3-CQA de 1,37 e 1,29% respectivamente, foi superior ao da testemunha, que permitiu obter um teor de 0,97% de 3-CQA. Verifica-se na tabela 6, que houve diferença significativa da atividade da enzima PPO da testemunha em relação às doses de Cu, em que a atividade da enzima PPO na testemunha foi superior às doses de Cu (0,05; 0,1; 0,2 e 0,4 µmol L-1), no entanto para a maior dose de Cu (0,8 µmol L-1) não houve diferença. Com base na classificação proposta por Carvalho et al. (1994) em função da PPO, pode-se atribuir aos grãos de café pulverizados com Cu, com atividade da PPO de 86,09 U. g-1 de amostra, a tratar-se de bebida “estritamente mole”.
Para os valores do índice de coloração (Tabela 6) houve diferença significativa da testemunha em relação a todas as doses de Cu, em que os valores do índice de coloração da testemunha foi superior aos valores determinados para as doses de Cu. Para o índice de coloração (IC) de grãos de café observou-se uma relação direta com a PPO, tendo a testemunha apresentado o maior valor IC (2,28 DO. 435nm) e maior atividade da enzima PPO.
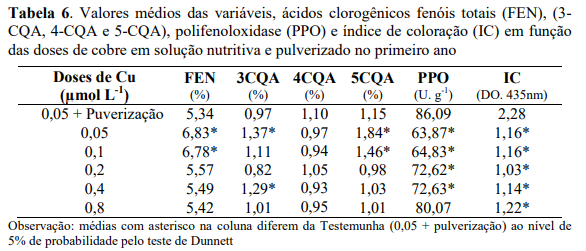
Cafeína e trigonelina
Os teores de trigonelina no primeiro ano se ajustaram ao modelo de raiz quadrada para as doses de cobre. Apresentando o maior teor de trigonelina (3,48 g 100 g-1) na dose estimada de 0,45 µmol L-1 e teor foliar de 4,5 mg kg-1 de Cu ( Υ 2,8444 3,7018Cu ˆ ; r 0,88 2 ), enquanto que na maior dose de Cu (0,8 µmol L-1) houve redução nos teores de trigonelina (2,77 g 100 g-1) (Figura 10). No segundo ano de avalição não se verificou efeito das doses de Cu para os teores de trigonelina.
Verificou-se, no primeiro ano que os teores de trigonelina não se relacionaram com a produção de grãos (Figura 3A), em que o maior teor de trigonelina (3,48 g 100 g1 ) na dose estimada (0,45 µmol L-1 de Cu) proporcionou uma baixa produção de grãos (14,44 g planta-1).
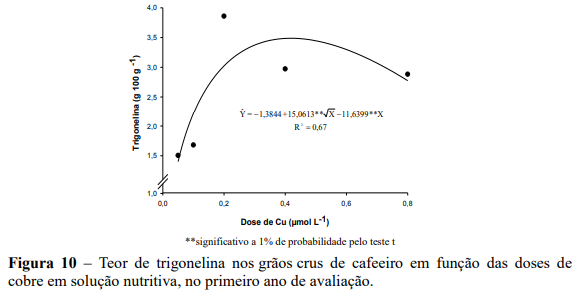
As maiores doses de Cu contribuíram expressivamente para o aumento no teor de trigonelina nos grãos de café (3,48 g 100 g-1). A enzima responsável pela formação de trigonelina via ácido nicotínico é a nicotinato N-metiltranferase também conhecida como trigonelina sintase (KOSHIRO et al., 2006; ASHIHARA, 2006). Como o Cu participa diretamente da formação de mais de cem enzimas e, indiretamente, da ativação de varias outras enzimas em plantas, em diversas rotas metabólicas e bioquímicas, pode estar envolvidos no processo de formação da trigonelina até certo limite.
Segundo Farah et al. (2006) a trigonelina é um dos precursores de produtos responsáveis pela qualidade do aroma do café, já que após a torra a degradação deste composto pode chegar até 90%, sendo a niacina o composto que se forma mais conhecido, como também as piridinas e alguns pirróis. O mesmo autor trabalhando com amostras de cafés de diferentes qualidades, observou que a redução da qualidade da bebida de café estava associada à redução dos níveis de trigonelina nos grãos.
Nos dois anos de avalição não se verificou efeito das doses de Cu para os teores de cafeína, porém, mesmo não tendo ocorrido diferença significativa entre as doses de Cu para a cafeína, observou-se uma tendência de aumento no seu teor do primeiro ano para o segundo ano de avaliação, tendo o primeiro ano apresentado teores médios variando de 0,99 a 1,37 g 100g-1 e no segundo ano de 1,30 a 1,47 g 100g-1 (Tabela 7).
Proantocianidinas
Para os teores de proantocianidinas, também não houve efeito significativo das doses de Cu em solução nutritiva nos dois anos de avaliação, verificando-se uma pequena variação no primeiro ano de 7,48 a 8,15 mg g-1 e no segundo ano de 6,17 a 6,26 mg g-1, com tendência de redução do primeiro ano para o segundo ano de avaliação. No entanto, os teores de proantocianidinas no presente trabalho foram superiores aos citados na literatura para o café arábica (MORAIS et al. 2009).
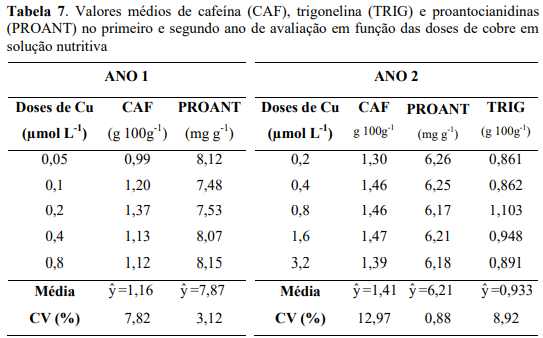
Observa-se na tabela 8, que houve diferença significativa das doses de Cu fornecidas via solução nutritiva em comparação com a testemunha, para as variáveis, cafeína, trigonelina e proantocianidinas. Os teores de cafeína na testemunha foram superiores aos da dose de Cu 0,5 µmol L-1 e não diferiram dos das demais doses (Tabela 8). A cafeína é a principal purina na composição do café e encontra-se no citoplasma e ligada à parede celular. Sem dúvida, esse alcalóide tem papel importante como estimulante (MENEZES, 1990). Segundo Illy e Viani (1995), a quantidade de cafeína presente no café é responsável por 10% de seu amargor, no entanto, o teor de cafeína não tem efeito direto na qualidade sensorial. Por outro lado, Franca, Mendonça e Oliveira, (2005) e Farah et al. (2006) encontraram maiores teores de cafeína em amostras de café arábica de alta qualidade, quando comparadas com as demais.
Os teores de trigonelina nas doses de Cu 0,05 e 0,1 µmol L-1 foram inferiores (1,50 e 1,68 g 100g-1) aos da testemunha (3,35 g 100g-1)(Tabela 8). A trigonelina (1- metil-3-carboxipiridina) está entre os alcaloides mais importantes do café. Sua degradação térmica gera pirróis e piridinas, relevantes para o flavor do café torrado. É produzida a partir do ácido nicotínico, mas em estágios avançados de germinação, parece ter função de reserva de ácido nicotínico para uma futura conversão à coenzima nicotinamida adenina dinucleotídico (NAD) (SHIMIZU; MAZZAFERA, 2000).
Para os teores de proantocianidinas, verifica-se que o valor observado no tratamento testemunha (7,12 mg g-1) diferiu dos observados nas doses de Cu (0,05; 0,4 e 0,8 µmol L-1) fornecidas via solucao (8,12; 8,07 e 8,15 mg g-1), (Tabela 8). Os teores de proantocianidinas no presente trabalho foram superiores aos citados na literatura para o café arábica (MORAIS et al. 2009). As proantocianidinas juntamente com os polifenóis apresentam sabor adstringente típico, são responsáveis pela adstringência da bebida do café (HASLAM, 1989; SILVA, 1991), interferindo no sabor e aroma do café após a torra.
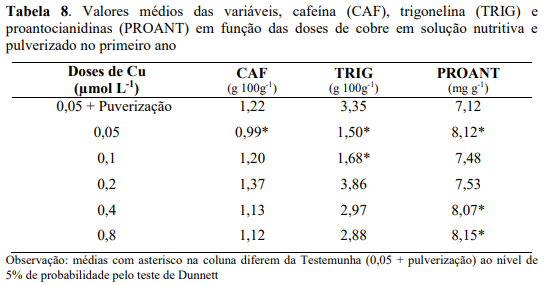
Sacarose
No primeiro ano o teor de sacarose apresentou efeito linear crescente com as doses de cobre. Na maior dose o teor de sacarose nos grãos crus foi igual a 7,94% (Figura 11A). O teor foliar de Cu que correspondeu ao ponto de máxima concentração de sacarose foi 5,8 mg kg-1 de Cu (Υ 2,8444 3,7018Cu ˆ ; r 0,88 2 ). Esse resultado corresponde ao incremento de 62% no teor de sacarose, em relação à menor dose de cobre, que permitiu obter o teor de 4,91% de sacarose. Este comportamento possivelmente esteja relacionado ao bom suprimento de cobre às plantas nas maiores doses, favorecendo com isso um maior transporte fotossintético de elétrons do PSII ao PSI, como consequência do aumento nos teores de plastocianina, na taxa de fixação de CO2, como também um maior teor de amido e de carboidratos solúveis (especialmente sacarose) nas plantas (KIRKBY e RÖMHELD, 2007).
No segundo ano de avaliação devido as modificações nas doses de Cu, o teor de sacarose apresentou incremento quadrático para as doses crescentes de Cu via solução nutritiva, verificando-se na dose estimada de 1,80 µmol L-1 de Cu, o maior teor de sacarose correspondente a 8,88% nos grãos crus de cafeeiro (Figura 11B), com teor foliar de Cu correspondendo a 8,85 mg kg-1 ( Υ 3,1025 3,1907Cu ˆ ; r 0,98 2 ). Esse resultado corresponde ao incremento de 21 % no teor de sacarose, em relação à menor dose de cobre, que permitiu aos grãos apresentarem 7,33% de sacarose. Para a dose máxima de Cu houve redução no teor de sacarose de 15% em comparação ao valor da dose estimada no ponto de máximo (8,88% de sacarose).
Na comparação da produção de grãos no primeiro ano de avaliação (Figura 3) com os teores de sacarose, observa-se uma relação direta, em que o maior teor de sacarose (7,94%) na maior dose de Cu (0,8 µmol L-1) coincidiu com a maior produção de grãos (22 g por planta). No segundo ano observou-se menor concordância da produção de grãos (Figura 3B) com os teores de sacarose, verificando-se na dose estimada de Cu (1,80 µmol L-1 maior teor de sacarose), uma pequena redução na produção de grãos (37,72 g por planta).
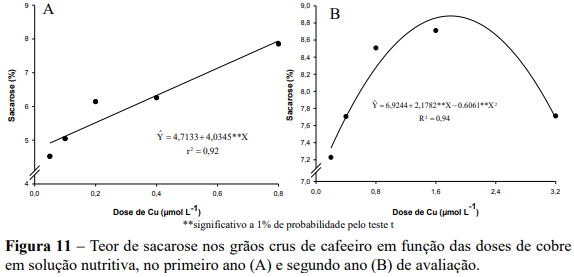
Cerca de 50% do Cu nas plantas estão nos cloroplastos, na plastocianina, onde participa da transferência de elétrons na fase fotoquímica da fotossíntese (HÄNSCH e MENDEL, 2009). Segundo Marschner, (2012), o aumento no fornecimento de Cu proporciona aumentos significativos de fotoassimilados para os grãos, em detrimento do rendimento da folhagem.
Esse aumento no teor de sacarose para as doses de cobre parece indicar que possivelmente esse micronutriente esteja também envolvidos na ativação da ligase da sacarose, enzima responsável pela acumulação desse açúcar em grãos de café arábico.
De acordo com Yruela, (2009) existem mais de cem enzimas em plantas que contem Cu. A sacarose é considerada uma característica de grande importância na qualidade da bebida, pois é um importante precursor do sabor e aroma do café. Os açúcares livres dominantes nos grãos de café são basicamente frutose, glicose e sacarose (ROGERS et al., 1999b). A sacarose representa quase todo açúcar livre nos grãos maduros de café.
Em C. arabica o teor de sacarose na matéria seca varia entre 5,1 e 9,4%, no grão maduro (CLIFFORD, 1985; KY et al., 2001; CAMPA et al., 2004). Segundo Franca et al. (2004), a qualidade final da bebida está intrinsecamente relacionada com a composição química dos grãos torrados, que é afetada pelas condições de processamento e pela composição química dos grãos crus de café.
Glicose, manose, arabinose e galactose
No primeiro ano de avalição não se verificou efeito das doses de Cu para os teores dos açucares redutores (manose, glicose, galactose e arabinose).
Observa-se pelos resultados (Figura 12A e 12B), que no segundo ano de avaliação, houve efeito das doses de cobre em solução nutritiva para os teores de arabinose e glicose. Com o aumento da dose de Cu, o teor de arabinose aumentou conforme o modelo de raiz quadrada com o maior teor (0,074%) verificado na dose estimada de 1,0 µmol L-1 de Cu (Figura 12A). Os teores foliares de Cu no ponto de máxima concentração de arabinose foram 6,29 mg kg-1 de Cu (Υ 3,1025 3,1907Cu ˆ ; r 0,98 2 ). Esse resultado corresponde ao incremento de 14% no teor de arabinose, em relação a menor dose de cobre (0,2 µmol L-1), no qual resultou o teor de 0,065%. Na dose máxima de Cu (3,2 µmol L-1) houve redução de 40% no teor (0,053%) em comparação ao valor da dose que permitiu valor máximo (0,074%).
Em relação aos teores de glicose, o aumento nas doses de Cu reduziu os teores de glicose, com o menor teor (0,13%) apresentado na dose estimada de 1,13 µmol L-1 de Cu e teor foliar de 6,70 mg kg-1 de Cu ( Υ 3,1025 3,1907Cu ˆ ; r 0,98 2 ) (Figura 12B). Enquanto que na dose máxima de Cu (3,2 µmol L-1) houve um incremento no teor de glicose de 85% (0,24 % de glicose) em comparação ao valor da dose estimada que proporcionou 0,13% de glicose.
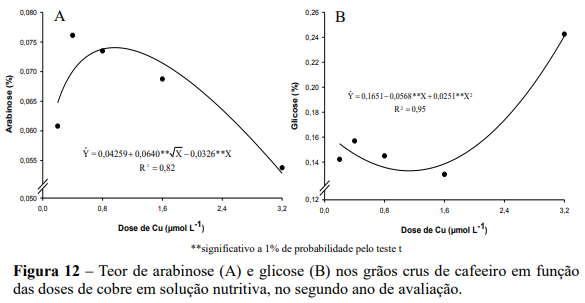
Dos açucares solúveis presentes nos grãos de café, destacam-se a glicose, frutose, manose, galactose e a sacarose, uma pequena porcentagem dos carboidratos presentes no grão. Estes, além de atuarem como reservas de utilização rápida constituem importante proteção, limitando os danos causados pela dessecação em sementes maduras (BUCKERIDGE et al., 2000).
Com isso, contribuem com a doçura da bebida do café, um dos atributos de sabor mais desejáveis nos cafés especiais, e participam de importantes reações (PEREIRA et al., 2002; CORADI et al., 2007; MARQUES et al., 2008). Segundo Mendonça et al. (2007), maior concentração de açúcares nos grãos crus de café contribuem, expressivamente, para as reações durante a torração.
Verifica-se na Tabela 9, que houve diferença significativa das doses de Cu fornecidas via solução nutritiva em relação à testemunha suplementada com pulverizações foliares para as variáveis sacarose (SAC), manose (MAN) e glicose (GLI), em que os teores dos açucares (sacarose, manose e glicose) da testemunha foram superiores aos das doses de Cu (0,05; 0,1; 0,2 e 0,4 µmol L-1). Enquanto que para a maior dose de Cu (0,8 µmol L-1) não houve diferença dos teores de açucares em relação à testemunha. Para galactose e arabinose também não observou diferença entre a testemunha e as doses de Cu.
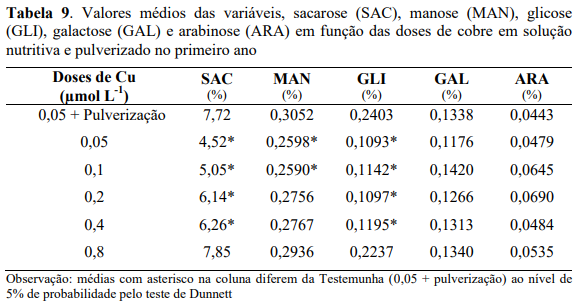
Esse aumento nos teores dos açucares (sacarose, manose e glicose) possivelmente esteja relacionado ao bom suprimento de cobre via pulverização foliar, favorecendo com isso um maior transporte fotossintético de elétrons, como consequência do aumento nos teores de plastocianina, na taxa de fixação de CO2, como também um maior teor de amido e de carboidratos solúveis (especialmente sacarose) nas plantas (KIRKBY e RÖMHELD, 2007). Cerca de 50% do Cu encontrado nas plantas está presente nos cloroplastos, presentes na plastocianina, onde participa do transporte de elétrons entre o PSII e PSI na membrana do tilacóide (HÄNSCH e MENDEL, 2009).
De modo geral, os teores dos açúcares totais descritos nesse trabalho encontramse numa faixa entre 5% e 8,5%, tendo a testemunha e a maior dose de Cu (0,8 µmol L-1) apresentado os maiores teores (8,43% e 8,54% respectivamente). Barrios (2001), Pinto (2002) e Villela (2002) afirmam que em cafés considerados bebida mole, apenas mole e estritamente mole estão entre 8,6 e 10% e Abrahão et al. (2009) observaram teores de açúcares solúveis totais em café cereja entre 7,06% e 7,71%.
Dos açúcares totais os redutores (manose, glicose, galactose e arabinose) estão presentes em menores quantidades (PEREIRA, 2002; PIMENTA; Vilela, 2002; RIBEIRO et al., 2003; SILVA et al., 2004; BORÉM et al., 2006; ABRAHÃO et al., 2009) pois, predominam os não redutores (sacarose). A concentração de sacarose pode variar de 1,9 a 10% na matéria seca (PEREIRA et al., 2002; LIMA, 2005; KNOPP et al., 2006; MENDONÇA et al., 2007). Maiores concentrações de açúcares no grão cru permitem um aumento na participação destes compostos nas reações do processo de torração (MENDONÇA et al., 2007), contribuindo com a doçura da bebida, que é considerado um dos atributos de sabor mais desejáveis nos cafés especiais (PEREIRA et al., 2002; CORADI et al., 2007; MARQUES et al., 2008). De acordo com Pereira et al. (2002); Coradi et al. (2007) e Marques et al.(2008), pode-se atribuir essa melhor qualidade às substâncias voláteis formadas a partir da combinação de tais açúcares com as proteínas no processo de torração.
Potássio lixiviado e condutividade elétrica
A quantidade de potássio lixiviado e a condutividade elétrica não variaram com a dose de Cu (Tabela 10). Os grãos de café com maior atividade da polifenoloxidase, apresentam tendência de maior IC, menor lixiviação de potássio e CE (CARVALHO et al., 1994), apesar de não diferirem para o KL e CE, em razão das doses de cobre (Tabela 9). Cafés de melhor qualidade possuem maior atividade da PPO e IC, menor KL e CE conforme pesquisas desenvolvidas por Carvalho et al. (1994), Leite & Carvalho (1994), Chagas et al. (1996), Silva et al. (2002) e Silva et al. (2009).
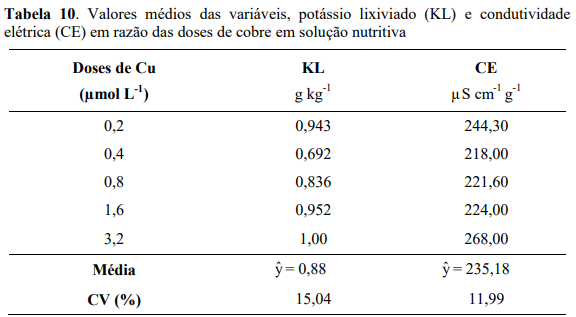
Os testes de condutividade elétrica e potássio lixiviado são utilizados como identificador da qualidade, porque apresentam maior sensibilidade na detecção de degradações nas membranas celulares dos grãos, pelo manejo inadequado nas fases de pré e pós-colheita (ANGÉLICO, 2008). Uma maior lixiviação de potássio, e consequente aumento na condutividade elétrica, é um bom indicador de danos na membrana e na parede celular (GOULART et al. 2007).
Levando-se em consideração os resultados obtidos no segundo ano de avaliação, em que as doses de Cu empregadas permitiram obter curvas de resposta de maior amplitude, observa-se que doses entre 1,45 e 2,59 µmol L-1 de Cu permitiram otimizar a produtividade e diversas características relacionadas à qualidade. Nessa faixa, produção de grãos e sacarose alcançaram valores máximos, enquanto que ATT, pH, fenóis totais, 5-CQA e 4-CQA alcançaram valores mínimos. Nessas condições os teores de Cu nas folhas índice estiveram entre 7,20 e 11,37 mg kg-1, ou seja, no limite inferior da faixa crítica determinada por MARTINEZ et al., 2003. Cabe salientar, entretanto, que essa faixa crítica foi obtida em condições de campo e apresenta a variabilidade inerente a tais condições, incluindo a presença de íons adsorvidos às cutículas foliares não eliminados no processo de lavagem das folhas que precede a análise, o que no presente estudo, em condições controladas, não ocorreu.
Merece destaque, ainda, o fato da atividade da PPO, importante definidora da qualidade, ter sido maximizada em grãos de plantas com 5,6 mg kg-1 de Cu nas folhas índice, ou seja, abaixo da faixa crítica proposta por MARTINEZ et al., 2003.
Análise sensorial
O café como bebida é normalmente classificado em sete grupos: estritamente mole, mole, apenas mole, dura, riada, rio e rio zona, sendo as quatro primeiras consideradas bebidas finas e as três últimas bebidas fenicadas. Certos atributos podem ser adicionados a classificação, provenientes de fermentações que podem levar à aquisição de características secundárias obtendo, assim, tipos de bebida tais como dura fraca, mole com bom corpo, doce e equilibrado entre outras. No presente trabalho características da bebida foram transformadas em escalas de valores permitindo uma avaliação quantitativa, como também foram incluídos suas classificações e atributos (Tabela 11).
Pela avaliação sensorial (prova de xícara) verificou-se que não houve diferença significativa entre as doses de Cu em solução nutritiva. No entanto, as maiores doses de Cu proporcionaram atributos diferentes das doses menores, mas de modo geral corresponderam à bebida mole (Tabela 11).
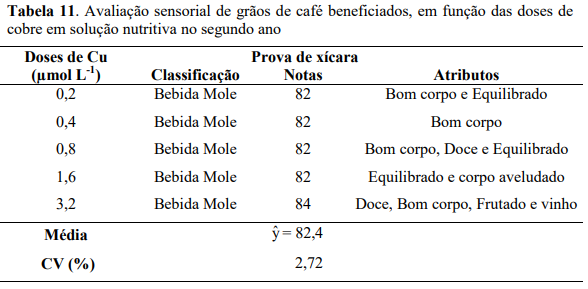
CONCLUSÕES
Doses de Cu entre 1,5 e 2,0 µmol L-1 via solução nutritiva permitiram maximizar nos dois anos de avaliação, a produção de grãos e os atributos químicos relacionadas à qualidade de bebida do café, como a atividade da PPO, os teores de sacarose, trigonelina, acidez titulável, arabinose, o isômero do ácido clorogênico (3-CQA), os ácidos tartárico, cítrico e málico. Doses inferiores, ou superiores permitiram o incremento dos atributos relacionados com a perda de qualidade da bebida como, os fenóis totais, o ácido 5-CQA, o pH, AT, e o isômero do ácido clorogênico (4-CQA). Os teores foliares que se relacionaram aos pontos de máximo ou mínimo dos atributos de qualidade estudados variaram entre 5,6 e 11,37 mg kg-1 de Cu, ou seja estão no limite inferior, ou abaixo da faixa de concentrações consideradas adequadas para o cafeeiro.
O fornecimento de Cu via foliar aumentou a produção de frutos, a atividade da PPO, os teores de sacarose, manose, glicose, trigonelina e cafeína, o índice de coloração, pH e os teores de ácido málico, atributos relacionados com a melhoria da qualidade da bebida do café, e, negativamente, fenóis totais, isômeros do ácido clorogênico (5-CQA) todos prejudiciais à qualidade da bebida de café.

Fonte
LACERDA,. Produção, composição química e qualidade da bebida de café arábica em razão da dose de cobre e zinco. Sbicafe.ufv.br, 2014. Disponível em: <http://www.sbicafe.ufv.br/handle/123456789/5549>. Acesso em: 12 dez. 2022.