Mecanismo de Ação: Inibidores do Fotossistema II (FSII)

São também conhecidos como inibidores da fotossíntese II ou síntese de Hill, por inibirem a evolução do oxigênio a partir da água na presença de cloroplastos e de um aceptor adequado de elétrons.
A ação seletiva destes compostos foi descoberta na década de 50, mas tais herbicidas constituem, até hoje, um dos mais numerosos e importantes grupos de herbicidas, com ampla utilização em diversas culturas.
A introdução de atrazine no início da década de 60 revolucionou a produção de milho, já que a partir de então um herbicida confiável para o controle de folhas largas nesta cultura passou a estar disponível.
Os inibidores da fotossíntese são considerados inibidores do transporte de elétrons (Balke, 1985), uma vez que resultam na remoção ou inativação de um ou mais carregadores intermediários do transporte de elétrons.
Características gerais
1. A taxa de fixação de CO2 declina poucas horas após o tratamento em plantas susceptíveis tratadas. Em plantas tolerantes, a taxa de fixação não cai a níveis tão baixos e em poucos dias retorna ao normal; nas sensíveis a taxa declina até próximo de zero em 1 ou 2 dias e não ocorre recuperação;
2. Aparentemente todos podem ser absorvidos via radicular e a maioria através das folhas. No entanto, quando utilizados em aplicações em pós-emergência, uma cobertura completa das plantas é importante, uma vez que a translocação é limitada. Adjuvantes são normalmente adicionados para aumentar a ação foliar;
3. Todos se translocam basicamente via xilema; portanto, plantas perenes só podem ser afetadas em aplicações via solo;
4. Plantas tornam-se mais susceptíveis a aplicações em pós-emergência quando baixa intensidade de luz ocorre durante os dias que precedem a aplicação e alta intensidade de luz ocorre nos dias posteriores;
5. Em geral o movimento no solo vai de baixo a moderado, embora possa variar de acordo com o composto e o solo. A persistência é extremamente variável, podendo variar de alguns dias até mais de um ano;
6. Interação sinergística geralmente ocorre quando aplicados ao mesmo tempo ou próximos à aplicação de inseticidas inibidores da colinesterase;
7. Controlam muitas espécies de folhas largas e algumas gramíneas.
Modo de ação
A inibição da fotossíntese acontece pela ligação dos herbicidas deste grupo ao sítio de ligação da QB, na proteína D1 do fotossistema II, o qual se localiza nas membranas dos tilacóides dos cloroplastos, causando, por consequência, o bloqueio do transporte de elétrons de QA para QB.
Isto interrompe a fixação de CO2 e a produção de ATP e NADPH2, os quais são elementos essenciais para o crescimento das plantas. A morte das plantas, entretanto, na maioria dos casos ocorre por causa de outros processos.
Os primeiros trabalhos sugeriam que as plantas morriam por “inanição”, como resultado da inibição da reação luminosa da fotossíntese.
No entanto, as plantas tratadas com inibidores da fotossíntese morrem mais rápido quando colocadas à luz do que quando são colocadas no escuro.
Isto prova que algo além da inibição da fotossíntese é responsável pelo efeito herbicida observado. Pensa-se que a clorose foliar que se desenvolve após o tratamento seja causada pela peroxidação de lipídeos.
Lipídeos e proteínas são oxidados, resultando em rompimento de membranas, o que faz com que células e organelas desidratem e desintegrem-se rapidamente.
A peroxidação dos lipídeos é autocatalítica e se espalha para outros lipídeos constituintes de membranas, como as do cloroplasto e de outras estruturas celulares.
Estas reações acabam por promover a destruição das membranas e a perda de clorofila, resultando no aumento de tamanho e da desorganização dos tilacóides e de outras membranas celulares (Bartels, 1985a).
O processo de peroxidação acontece basicamente pela interrupção do fluxo de elétrons no fotossistema II, o que gera um estado energético tão elevado da clorofila (estado triplet), que sobrecarrega o efeito de atenuação de energia promovido pelos pigmentos carotenoides.
O excesso de clorofila triplet pode iniciar o processo de peroxidação de lipídeos por meio de dois mecanismos (Dan Hess, 1994b): o primeiro é a formação direta de radicais lipídicos nos ácidos graxos insaturados constituintes das membranas.
O segundo é que a clorofila triplet pode reagir com o oxigênio para produzir oxigênio singlet. O oxigênio pode então reagir com estes radicais para iniciar o processo de peroxidação que resulta no dano às membranas.
Locais de atuação nas plantas
Considera-se que existam três formas de ligação dos herbicidas à proteína D1, as quais formam subgrupos dentro deste mecanismo de ação.
O primeiro subgrupo é composto por herbicidas dos grupos químicos fenilcarbamatos, piridazinonas, triazinas, triazinonas, triazolinonas e uracilas -C1(5); o segundo, pelos herbicidas dos grupos amidas e ureias - C2(7); e o terceiro pelos herbicidas dos grupos benzotiadiazinonas, nitrilas e fenilpiridazinas - C3(6).
Independente do sítio específico de ligação, estes herbicidas apresentam sintomas semelhantes de progressão de injúrias nas plantas susceptíveis.
O diuron e outros derivados da ureia ligam-se a proteínas de peso molecular definido no “sítio da ureia”, enquanto outros herbicidas, especialmente as triazinas, ligam-se a proteínas de uma forma diferente. O sítio de ligação de ambos na cadeia de transporte de elétrons do cloroplasto é indicado na Figura 1.
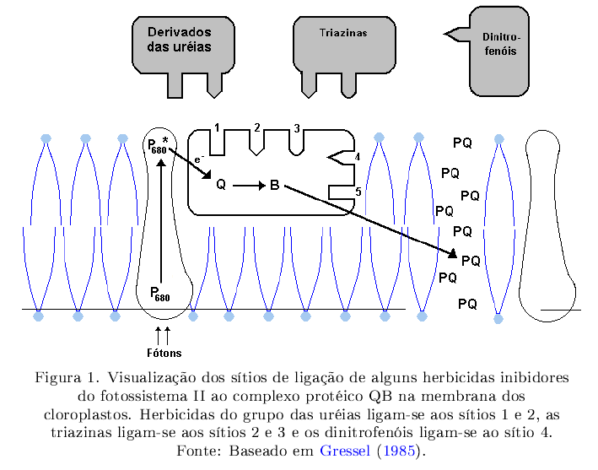
Um terceiro sítio, não descrito na Figura 1, é o local de atuação das benzotiadiazinonas, nitrilas e fenilpiridazinas. Existe ainda uma outra família de inibidores fotossintéticos que também se liga ao grupamento QB.
São os chamados inibidores “não clássicos”, constituídos pelos dinitrofenóis (Figura 1). Recentemente alguns derivados dos dinitrofenóis têm sido descritos como inibidores da fotossíntese, como por exemplo as pyridazinonas (norflurazon) e quinolinas (quinclorac).
No entanto, considera-se que a atuação dos fenóis sobre a fotossíntese constitua apenas um evento secundário na toxicidade destes herbicidas para as plantas.
Seletividade
As triazinas simétricas como atrazine são degradadas em muitas plantas tolerantes ao metabolismo do herbicida, especialmente pelo processo de conjugação com glutationa nas folhas, o que faz com que ele nunca chegue ao cloroplasto para causar injúrias.
Espécies como milho, Panicum miliaceum, Panicum dichotomiflorum, Digitaria spp. E Setaria spp. São especialmente adaptadas a fazer este processo de destoxificação (University of Minnesota, 2009).
Além do processo de metabolismo, uma série de fatores, isolados ou em conjunto, pode ser responsável pela seleção de plantas tolerantes ou susceptíveis a herbicidas deste grupo:
- Localização no solo (seletividade de posição);
- Aplicação dirigida;
- Absorção diferencial por raízes ou folhas;
- Translocação diferencial das raízes para as folhas;
- Sorção em sítios inativos nas plantas;
- Dentro de uma mesma variedade, sementes maiores tem maior tolerância;
Grupos químicos e herbicidas
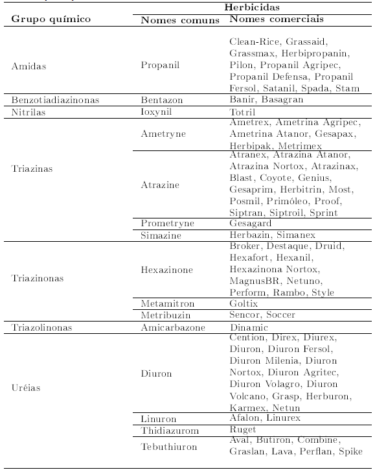
Principais misturas
- Ametryne+diuron+MCPA: Agritrin
- Ametryne+diuron: Ametron, Bimetron
- Ametryne+trioxysulfuron: Krismat
- Ametryne+simazine: Simetrex, Topeze
- Ametryne+clomazone: Sinerge
- Alachlor+atrazine: Agimix, Alaclor+Atrazina Nortox, Alazine, Boxer
- Atrazine+simazine: Atramix, Atrasimex, Bench, Extrazin, Herbimix, Primatop, Senior, Simtrac, Triamex
- Atrazine+glyphosate: Gillanex
- Atrazine+s-metolachlor: Primagram Gold, Primaiz, Primestra Gold
- Atrazine+nicosulfuron: Sanson AZ
- Bentazon+dicloreto de paraquat: Pramato
- Bentazon+imazamox: Amplo
- Bromacil+diuron: Krovar
- Clomazone+hexazinone: Discover, Ranger
- Diuron+dicloreto de paraquat: Gramocil
- Diuron+glyphosate: Glydur, Tropuron
- Diuron+hexazinone: Advance, Avelex, Confidence, Coronel BR, Dihex, Dizone, Help, Hexaron, Hexazinona-D Nortox, Jump, Rancho, Scopus, Soldier, Velpar Max, Velpar K, Xekil
- Diuron+hexazinone+sulfometuron: Front
- Diuron+tebuthiuron: Bimate
- Diuron+thidiazuron: Dropp Ultra
- Diuron+MSMA: Fortex
- Glyphosate+simazine: Tropazin
Outros princípios ativos com o mesmo mecanismo de ação, mas que não são registrados para uso no Brasil incluem pentanochlor (amidas), bromofenoxim, bromoxynil (nitrilas), cyanazine, desmetryne, dimethametryn, prometon, propazine, simetryne, terbumeturon, terbutylazine, terbutryne, trietazine (triazinas), bromacil, lenacil, terbacil (uracilas), chloridazon (piridazinonas), desmedipham, phemedipham (fenilcarbamatos), chlorobromuron, chlorotoluron, chloroxuron, dimefuron, ethidimuron, fenuron, fluometuron, isoproturon, isouron, metobromuron, metabenzthiazuron, metoxuron, monolinuron, neburon, siduron (ureias) e pyridafol e pyridate (fenilpiridazinas).
O bentazon, muito embora esteja incluído entre os inibidores do fotossistema II, apresenta muitas características em comum com os inibidores do fotossistema I:
- É utilizado apenas em pós-emergência, devido à absorção primariamente foliar e à pequena capacidade de translocação. Os efeitos de injúria nas plantas manifestam-se próximos ou nos locais pulverizados, ou seja, é considerado um herbicida de contato;
- As plantas são mais sensíveis quando mais tecidos tenros estão presentes;
- Algumas culturas nas quais é usado podem evidenciar injúrias relativamente severas (necrose), mas recuperam-se após certo tempo, uma vez que não apresenta translocação e nem efeito residual no solo;
- A dessecação do tecido foliar e perda da capacidade fotossintética leva à paralisação do crescimento e à morte.
Se você tem interesse em saber mais sobre a Utilização de Herbicidas na Agricultura, te convido a conhecer a plataforma da AgricOnline. Ao fazer a sua assinatura, você tem acesso ilimitado a todos os cursos da plataforma. São cursos que vão desde produção vegetal, produção animal, mercado e carreira.
Ao término de cada curso, você tem direito ao certificado com a carga horária de cada curso, clique no link para conhecer.

Ou clique no link:
https://go.agriconline.com.br/pass/?sck=portal
Fonte
DE OLIVEIRA, Rubem Silvério Júnior; CONSTANTIN, Jamil; INOUE, Miriam Hiroko. Biologia e Manejo de Plantas Daninhas. Curitiba - PR: Ommipax, 2011.