A Acidez do Solo

Acidez do Solo
A reação do solo é o primeiro fator que precisa ser conhecido em uma área a ser cultivada. Isso porque, caso ela não seja favorável às culturas, devem ser tomadas medidas corretivas com antecedência.
A condição desfavorável de reação do solo mais comum nos solos brasileiros é a acidez excessiva, assim a correção dos solos pela calagem é uma prática fundamental, nas condições em que as culturas respondem a essa atividade (QUAGGIO, 1986; RAIJ, 1991).
Existem, atualmente, técnicas seguras para caracterizar a acidez dos solos e para avaliar a necessidade de calagem, permitindo dimensionar as quantidades de corretivos para a exigência diferenciada de culturas (RIBEIRO; GUIMARÃES; ALVAREZ, 1999).
Conceitos e Componentes da Acidez
Do ponto de vista químico, ácidos são substâncias que, em solução, liberam prótons (íons hidrogênio). Ao contrário, bases são substâncias capazes de receber prótons.
Em solos, os sistemas de interesse são em geral aquosos e pode-se utilizar, com vantagem, as expressões em íons hidrogênio (H+) e hidróxido (OH-). A dissociação de um ácido em solução pode ser representada por: HA ⇔ H+ + A- (ALCARDE, 2005; MEURER, 2010).
O ácido HA dissocia-se no cátion H+ e no ânion (simbólico) A- – ácidos fortes dissociam-se completamente – enquanto os ácidos fracos dissociam-se pouco.
Em condições normais, a reação ácida do solo tende a ser similar à dos ácidos fracos. Nem todos os H+ do solo estão em solução (dissociáveis), ao contrário, estão em pequena quantidade, pois a grande reserva está adsorvida no complexo de troca (BOHNEN, 2000; SUMNER, 1997).
O fato de ácidos fracos se dissociarem pouco ocorre em soluções concentrações muito baixas, tão baixas que seria difícil representá-las na notação de frações decimais. O conceito de pH, introduzido para representar concentrações efetivas (do íon H+) muito baixas de íons hidrogênio, é definido por:
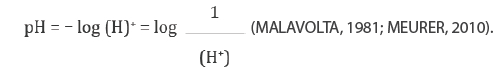
Como exemplo, uma concentração 0,00001 mol L-1 ou 10-5 mol L-1 de H+ corresponderia a:
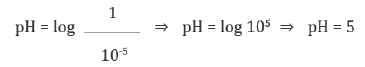
A escala de pH varia de 0 a 14. Em solos, podem ser encontrados valores de menos de 3 até cerca de 9, embora os valores mais comuns ocorram na faixa intermediária.

Reações do Solo
As reações do solo podem ser:
a) reação ácida (pH<7,0): em solos distribuídos nas regiões de alta pluviosidade, os elementos alcalinos Na, Ca, Mg, K, são lixiviados e substituídos por íons H+ e Aℓ3+;
b) reação básica (pH>7,0): em solos distribuídos nas regiões áridas (evapotranspiração maior que precipitação), ocorrem condições favoráveis para o acúmulo de elementos alcalinos na solução do solo, e um predomínio de íons OH- sobre os íons H+;
c) reação neutra (pH = 7,0): em solos normais, os valores de pH geralmente encontram-se no intervalo de 4,0 a 7,0 (ASSOCIAÇÃO BRASILEIRA PARA PESQUISA DA POTASSA E DO FOSFATO, 1998).
Tipos de Acidez (Acidez Ativa e Potencial)
Os solos apresentam diversos componentes que possuem a propriedade de troca iônica. Essa capacidade de troca de cátions dos solos é contrabalançada, em parte, por cátions trocáveis, existindo também grupamentos ionogênicos (posições na estrutura sólida que apresentam ou podem liberar cargas elétricas negativas) ocupados por hidrogênio não dissociado.
Os tipos de acidez do solo são os seguintes (RAIJ; QUAGGIO, 1997):
a) acidez ativa;
b) acidez potencial (trocável e não trocável).
Acidez ativa (H+ na solução no solo)
É a acidez devida à concentração de íons de hidrogênio (H+) que se encontram livres ou dissociados na solução do solo, fase líquida (Figura 25).
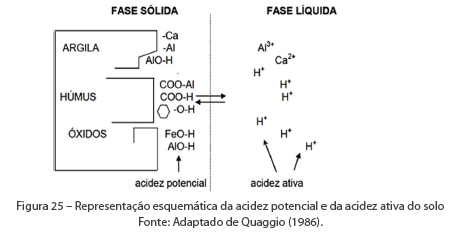
A determinação mais comum em amostras de solo é a que estima a atividade do íon H+, o pH. Determina-se a atividade dos íons H+ em suspensão com água ou solução salina.
A acidez ativa é medida pelo pH. Por exemplo:
pH = 6,0 = 10-6 mol L-1 H+
Como ela representa íons na fase líquida, a atividade de H+ muito baixa, como por exemplo, pHCaCℓ2 = 4,0 que corresponderia a uma atividade de íons H+ na fase líquida igual a 0,0001 mol L-1 (QUAGGIO, 1986; RAIJ et al., 2001; MEURER, 2010).
Métodos de determinação da acidez ativa
O método colorimétrico baseia-se na capacidade de certas substâncias químicas (compostos orgânicos ou alcalinos fracos) de desenvolver uma coloração conhecida, de acordo com o pH da solução.
Utilizam indicadores ácido-base na forma de fitas ou soluções que mudam de cor pela atividade do íon H+ (Tabela 7). São métodos rápidos, apresentando apenas o inconveniente de ser pouco precisos.

O método potenciométrico é a medida da concentração efetiva dos íons H+ na suspensão do solo. O conjunto medidor e eletrodo de vidro combinado é conhecido como potenciômetro ou peagâmetro.
O detector é constituído de um eletrodo indicador de vidro, sensível a variações de H+ da solução. O outro eletrodo, que é inerte a estas oscilações, é o eletrodo de referência. A diferença de potencial entre eletrodo indicador e eletrodo de referência é registrada por um medidor, sendo apresentada em Volt ou diretamente em pH.
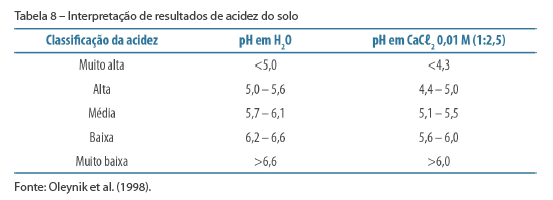
Interpretação dos resultados para acidez do solo
A Tabela 8 apresenta a interpretação dos resultados de acidez do solo para os dois métodos de análise.
Solos eletropositivos e eletronegativos
Para determinar se o solo é eletronegativo ou eletropositivo estimasse o valor de ΔpH. Este índice fornece a ideia do grau de intemperização do solo e é calculado pela equação:
ΔpH = pH (KCℓ) – pH (H2O)
ΔpH é negativo para solos eletronegativos. É o caso mais comum, indicando que o solo tem predominância de cargas negativas e que uma parte delas está ocupada pelo H+ e Aℓ3+ (GIANELLO; BISSANI; TEDESCO, 1995; SILVA, 2009).
Em solos eletronegativos, o pH diminui com a concentração salina da solução:
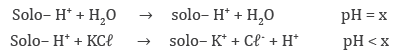
ΔpH é positivo para solos eletropositivos. Isso pode ocorrer em horizontes mais profundos de solos muito intemperizados, com altos teores de óxidos e hidróxidos de Fe e Aℓ.
Em solos eletropositivos, o pH aumenta com a concentração salina da solução, isso acontece em razão da troca entre o ânion do sal e OH- na superfície das argilas.
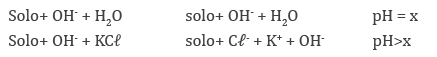
Acidez potencial (H+ + Aℓ³+)
Os componentes da acidez potencial, os íons de Aℓ³+ e H+, diferem quanto ao modo de se ligar ao complexo coloidal. No caso do Aℓ3+, as ligações são predominantemente eletrostáticas. Isso significa que os íons Aℓ3+ podem ser deslocados dos sítios de adsorção por simples troca iônica.

Os íons de Aℓ3+ são chamados de trocáveis, e a acidez por eles gerada é denominada de acidez trocável (RAIJ et al., 2001). Os íons H+ estão ligados à fase sólida do solo, através de ligações covalentes, que são bem mais estáveis do que as ligações eletrostáticas.
Devido a este fato, a extração dos íons H+ do complexo coloidal requer uma reação mais enérgica do que a troca iônica.
Emprega-se a solução de acetato de cálcio 0,5 mol L-1 a pH 7,0 para extrair os íons H+ e consequentemente são extraídos também os Aℓ3+. O conjunto destes íons é denominado de acidez potencial (RIBEIRO; GUIMARÃES; ALVAREZ, 1999).
A acidez potencial divide-se em:
a) acidez trocável: refere-se aos íons Aℓ3+ e H+ retidos na superfície dos colóides do solo. Esta quantidade de H+ trocável é pequena. Como o H+ representa menos de 5% da acidez trocável, é admitido apenas o Aℓ3+ trocável; a acidez trocável (cmolc dm-3 ou mmolc dm-3): refere-se ao alumínio (Aℓ3+) e hidrogênio (H+) trocáveis e adsorvidos nas superfícies dos colóides minerais ou orgânicos por forças eletrostáticas;
b) acidez não trocável: é o íon H+ de ligação covalente associado aos colóides em carga negativa e aos compostos de alumínio. É a acidez que os solos apresentam quando em pH menor que 5,5.
Acima de pH 5,5 não existe mais Aℓ3+ trocável. Acidez não trocável (cmolc dm-3 ou mmolc dm-3) é a quantidade de acidez titulável que ainda permanece no solo, após a remoção da acidez trocável com uma solução de um sal neutro não-tamponado, como KCℓ 1 mol L-1.
Esse tipo de acidez é representado por H+ em ligação covalente (mais difícil de ser rompida) com as frações orgânicas e minerais do solo. A acidez potencial é a soma da acidez trocável e da acidez não trocável.
É ela que limita o crescimento das raízes e ocupa espaços nos colóides, possibilitando que os nutrientes livres na solução do solo sejam lixiviados (GIANELLO; BISSANI; TEDESCO, 1995; TEDESCO et al., 1995; RAIJ et al., 2001).
Se você tem interesse em saber mais sobre a Fertilidade do Solo, te convido a conhecer a plataforma da AgricOnline. Ao fazer a sua assinatura, você tem acesso ilimitado a todos os cursos da plataforma. São cursos que vão desde produção vegetal, produção animal, mercado e carreira.
Ao término de cada curso, você tem direito ao certificado com a carga horária de cada curso, clique no link para conhecer.

Ou clique no link:
https://go.agriconline.com.br/pass/?sck=portal
Fonte
MENEGHETTI, Adriana Maria. Manual de Procedimentos de Amostragem e Análise Química de Plantas, Solo e Fertilizantes. 1ª ed. Curitiba - PR: EDUTFPR, 2018.